Aktivni sastojci: Lidokain
Versatis 5% ljekovita žbuka
Zašto se koristi Versatis? Čemu služi?
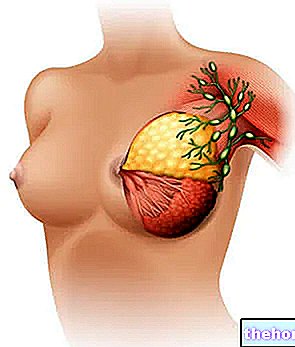
Versatis sadrži lidokain, lokalni analgetik, koji djeluje tako što smanjuje bol u koži. Propisano vam je za liječenje boli uzrokovane postherpetičnom neuralgijom. Ovo stanje općenito karakteriziraju lokalizirani simptomi poput pečenja, probadajuće ili probadajuće boli.
Kontraindikacije Kada se Versatis ne smije koristiti
Nemojte koristiti Versatis
- ako ste alergični na lidokain ili neki drugi sastojak ovog lijeka (naveden u odjeljku 6)
- ako ste imali alergijsku reakciju na druge proizvode slične lidokainu, kao što su bupivakain, etidokain, mepivakain ili prilokain
- na slomljenoj koži ili otvorenim ranama.
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Versatis
Prije upotrebe Versatisa razgovarajte sa svojim liječnikom ili ljekarnikom Ako imate tešku bolest jetre ili imate teške probleme sa srcem ili bubrezima, prije upotrebe Versatisa razgovarajte sa svojim liječnikom. Versatis se treba nanositi na kožu nakon zarastanja lezija šindre. Ne smije se nanositi na ili u blizini očiju ili usta.
Lidokain se u jetri metabolizira u brojne spojeve. Jedan takav spoj je 2,6 ksilidin za koji se pokazalo da uzrokuje tumore kod štakora ako se daje kontinuirano u vrlo visokim dozama. Vrijednost ovih podataka kod ljudi nije poznata.
Djeca i adolescenti
Versatis nije ispitivan u bolesnika mlađih od 18 godina, stoga se uporaba u tih bolesnika ne preporučuje.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak lijeka Versatis
Obavijestite svog liječnika ili ljekarnika ako uzimate ili ste nedavno uzimali ili biste mogli uzeti bilo koje druge lijekove.
Upozorenja Važno je znati da:
Trudnoća, dojenje i plodnost
Ako ste trudni, mislite da ste trudni ili planirate trudnoću, ili ako dojite, pitajte svog liječnika ili ljekarnika za savjet prije nego počnete koristiti ovaj lijek. Versatis se ne smije koristiti tijekom trudnoće, osim ako je to nužno potrebno. nema studija o upotrebi flastera tijekom dojenja. Kada se koristi Versatis, samo mala količina aktivnog sastojka, lidokaina, može biti prisutna u krvi. Učinak na dojene bebe nije vjerojatan.
Upravljanje vozilima i strojevima
Učinak lijeka Versatis na sposobnost upravljanja vozilima i rada sa strojevima nije vjerojatan. Stoga je tijekom vožnje Versatisom moguće upravljati vozilima ili raditi na strojevima.
Versatis sadrži propilen glikol, metil parahidroksibenzoat i propil parahidroksibenzoat.
Flasteri sadrže propilen glikol (E1520) koji može izazvati iritaciju kože. Osim toga, sadrže metil parahidroksibenzoat (E218) i propil parahidroksibenzoat (E216) koji mogu izazvati alergijske reakcije. Ponekad se nakon određenog vremenskog razdoblja mogu pojaviti alergijske reakcije.
Doza, način i vrijeme primjene Kako se koristi Versatis: Doziranje
Uvijek koristite ovaj lijek točno onako kako vam je rekao liječnik. Ako ste u nedoumici, obratite se svom liječniku ili ljekarniku. Obično je dnevna doza jedna do tri zakrpe veličine područja bolne kože. Versatis se može izrezati na manje komade kako bi pokrio zahvaćeno područje. Ne smijete koristiti više od 3 zakrpe istovremeno. Zakrpe se moraju ukloniti nakon 12 sati primjene; to će vam dati period od 12 sati bez zakrpa. Možete odabrati želite li primijeniti Versatis danju ili noću. Općenito ćete osjetiti olakšanje boli od prvog dana korištenja, ali može proći i do 2-4 tjedna da učinak Versatisa ublaži bol bude potpun. Ako je nakon tog vremena bol i dalje vrlo intenzivna, obavijestite svog liječnika jer se korist liječenja mora odmjeriti s mogućim rizicima (pogledajte "Upozorenja i mjere opreza").
Vaš liječnik će u redovitim intervalima provjeravati djeluje li Versatis.
Prije nanošenja Versatis -a na zahvaćeno područje
- ako je bolno područje kože prekriveno kosom ili dlakom, potrebno ga je odrezati škarama.Ne smiju se brijati.
- Koža mora biti čista i suha.
- Kreme ili losioni mogu se koristiti na tretiranoj koži samo u razdoblju u kojem se flaster ne stavlja.
- Ako ste se upravo okupali ili istuširali, prije nanošenja flastera trebate pričekati da se koža ohladi.
Nanesite flaster
Korak 1: Otvorite vrećicu i uklonite jednu ili više zakrpa
- poderati ili izrezati omotnicu po isprekidanoj liniji
- ako koristite škare, pazite da ne oštetite zakrpe
- uzmite jedan ili više flastera, ovisno o veličini bolnog područja kože
Korak 2: Zatvorite omotnicu
- dobro zatvorite vrećicu nakon upotrebe
- flaster sadrži vodu i može se osušiti ako vrećica nije dobro zatvorena
Korak 3: Ako je potrebno, izrežite flaster
- ako je potrebno, prije uklanjanja filma, odrežite flaster na veličinu potrebnu da prekrije bolno područje kože.
Korak 4: Uklonite film
- uklonite prozirni film s flastera
- pokušajte ne dotaknuti ljepljivi dio flastera
Korak 5: Nanesite flaster i čvrsto pritisnite na kožu
- nanesite do tri flastera na bolno područje kože
- pritisnite flaster na kožu
- pritisnite i držite flaster najmanje 10 sekundi kako bi se flaster dobro prilijepio za kožu
- pobrinite se da sav flaster, uključujući rubove, prianja uz kožu.
Ostavite flaster na samo 12 sati
Važno je da se Versatis nanese na kožu samo 12 sati. Na primjer, ako tijekom noći osjećate veću bol, flaster možete staviti u 19 sati i ukloniti u 7 sati ujutro. Ako tijekom dana osjetite veću bol, možete nanijeti Versatis u 7 ujutro i skinuti ga u 7 navečer.
Kupka, tuširanje i kupanje
Budući da se mora izbjegavati kontakt Versatis -a s vodom, bilo koje kupke, tuširanje ili kupanje mogu se obavljati u razdoblju u kojem se flaster ne stavlja.Poslije kupanja ili tuširanja kožu je potrebno pustiti da se ohladi prije korištenja flastera.
Ako flaster otpadne
Vrlo rijetko se flaster može odlijepiti ili ne prianjati dobro. Ako je tako, pokušajte ga ponovno spojiti na isto područje. Ako se ne lijepi, potpuno ga uklonite i nanesite novi flaster, uvijek na isto mjesto.
Kako ukloniti Versatis
Za promjenu flastera polako skinite stari flaster. Ako se ne skida lako, možete ga namočiti vrućom vodom nekoliko minuta prije skidanja.
Predoziranje Što učiniti ako ste uzeli previše Versatisa
Ako ste zaboravili ukloniti flaster nakon 12 sati
Skinite flaster čim se sjetite. Novi flaster može se staviti nakon 12 sati.
Ako upotrijebite više flastera nego što ste trebali
Ako koristite više flastera nego što je potrebno ili ih držite predugo, rizik od nuspojava može se povećati.
Ako ste zaboravili primijeniti Versatis
Ako ste zaboravili staviti novi flaster nakon 12-satne stanke bez prethodnog, zalijepite ga čim se sjetite.
Ako imate dodatnih pitanja o uporabi ovog lijeka, obratite se svom liječniku ili ljekarniku.
Nuspojave Koje su nuspojave lijeka Versatis
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih. Ako tijekom nanošenja flastera postoji bilo kakva iritacija ili osjećaj peckanja, flaster treba ukloniti. Nemojte stavljati drugi flaster na to područje dok iritacija ne zacijeli.
Vrlo česte nuspojave koje se mogu javiti u više od 1 na 10 osoba navedene su u nastavku.
To uključuje promjene na koži na području primjene flastera ili blizu njega, a mogu uključivati crvenilo, osip, svrbež, peckanje, dermatitis i mjehuriće.
Manje česte nuspojave koje se mogu javiti u do 1 na 100 osoba navedene su u nastavku.
Promjene na koži i rane
U nastavku su navedene vrlo rijetke nuspojave koje se mogu javiti u do 1 na 10 000 osoba.
Otvorene rane, teške alergijske reakcije i alergija.
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku ili ljekarniku.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Također možete prijaviti nuspojave izravno putem nacionalnog sustava za prijavljivanje na http://www.agenziafarmaco.gov.it/it/responsabili.Prijavljivanjem nuspojava možete pomoći u pružanju više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
Čuvajte ovaj lijek izvan pogleda i dohvata djece. Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na vrećici i kutiji iza oznake EXP. Rok valjanosti odnosi se na zadnji dan tog mjeseca. Nemojte držati u hladnjaku ili zamrzivaču. Pažljivo zatvorite vrećicu nakon prvog otvaranja. Nakon otvaranja vrećice, flasteri se moraju upotrijebiti u roku od 14 dana. Nemojte koristiti ovaj lijek ako primijetite da je vrećica oštećena. Ako je tako, flaster se možda osušio i stoga se ne lijepi dobro.
Kako ukloniti Versatis
Korišteni flasteri i dalje sadrže aktivni sastojak koji bi mogao biti opasan za druge. Preklopite stare zakrpe na pola, s ljepljivom stranom iznutra, i bacite ih tako da ostanu izvan dohvata djece.
Nemojte bacati lijekove u otpadne vode ili kućni otpad. Pitajte ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Sastav i farmaceutski oblik
Što Versatis sadrži
- aktivni sastojak je lidokain
- svaki flaster 10 cm x 14 cm sadrži 700 mg (5% w / w) lidokaina
- ostale komponente u flasteru (pomoćne tvari) su: glicerol, sorbitol koji se može kristalizirati, natrij karmeloza, propilen glikol (E1520), urea, teški kaolin, vinska kiselina, želatina, polivinil alkohol, aluminij glicinat, dinatrijev edetat, metil parahidroksibenzoat (E218) , propil parahidroksibenzoat (E216), poliakrilna kiselina, natrijev poliakrilat, pročišćena voda.
Noseći sloj i ljepljivi sloj: polietilen tereftalat (PET).
Opis izgleda Versatis i sadržaj pakiranja
Ljekoviti flasteri dugi su 14 cm i široki 10 cm. Bijele su boje, od mekog materijala i nose natpis "lidokain 5%". Zakrpe su pakirane u vrećice koje se mogu ponovno zatvoriti, a svaka sadrži 5 zakrpa.
Svako pakiranje sadrži 5, 10, 20, 25 ili 30 flastera pakiranih u 1, 2, 4, 5 ili 6 vrećica.
Nisu sva pakiranja komercijalno dostupna.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA
VERSATIS 5% LIJEKOVITI AMBLEM
02.0 KVALITATIVNI I KOLIČINSKI SASTAV
Svaki flaster veličine 10 x 14 cm sadrži 700 mg (5% w / w) lidokaina (50 mg lidokaina / gram ljepljive baze)
Pomoćne tvari s poznatim učinkom:
Metil parahidroksibenzoat 14 mg
Propil parahidroksibenzoat 7 mg
Propilen glikol 700 mg
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK
Ljekovita žbuka
Bijeli hidrogelni flaster koji sadrži ljepljivi materijal nanesen na netkanu podlogu od polietilen tereftalata s utisnutim natpisom "Lidokain 5%" i prekriven zaštitnim filmom od polietilen tereftalata.
04.0 KLINIČKI PODACI
04.1 Terapeutske indikacije
Versatis je indiciran za simptomatsko liječenje neuropatske boli povezane s prethodnom infekcijom herpes zostera (postherpetična neuralgija, NPH) u odraslih.
04.2 Doziranje i način primjene
Odrasli i starije osobe
Bolno područje mora biti prekriveno flasterom, nanijeti jednom dnevno ne duže od 12 sati u roku od 24 sata. Treba staviti samo flastere potrebne za učinkovito liječenje. Po potrebi se flaster može rezati na manje dijelove škarama prije uklanjanja zaštitnog filma. Ukupno se ne smiju nanositi više od tri zakrpe istodobno.
Flaster se mora nanijeti na netaknutu, suhu i ne iritiranu kožu (nakon zacjeljivanja herpetičnih lezija).
Svaki flaster se ne može staviti duže od 12 sati. Slobodni interval od sljedeće primjene trebao bi biti najmanje 12 sati. Flaster se može staviti danju ili noću.
Flaster se mora nanijeti na kožu odmah nakon uklanjanja iz vrećice i uklanjanja zaštitnog filma s površine hidrogela. Kosa i kosa u području primjene moraju se ošišati škarama (ne obrijane).
Liječenje treba ponovno procijeniti nakon 2-4 tjedna. Ako nakon tog razdoblja nije bilo terapijskog odgovora na Versatis (tijekom primjene flastera i / ili razdoblja bez flastera, liječenje treba prekinuti jer bi u ovoj situaciji potencijalni rizici mogli premašiti koristi (vidjeti dijelove 4.4 i 5.1). Dugotrajna uporaba lijeka Versatis u kliničkim ispitivanjima pokazala je da se broj flastera koji se koriste s vremenom smanjuje. Stoga je potrebno redovito procjenjivati liječenje kako bi se odlučilo treba li broj flastera koji su potrebni za pokrivanje bolnog područja može se smanjiti ili može li se povećati slobodni interval između nanošenja flastera.
Oštećenje bubrega
U bolesnika s blagim ili umjerenim oštećenjem bubrega nije potrebno prilagođavanje doze. Versatis se mora koristiti s oprezom u bolesnika s teškim oštećenjem bubrega (vidjeti dio 4.4)
Oštećenje jetre
U bolesnika s blagim ili umjerenim oštećenjem jetre nije potrebno prilagođavanje doze. Versatis se mora koristiti s oprezom u bolesnika s teškim oštećenjem jetre (vidjeti dio 4.4).
Pedijatrijska populacija
Sigurnost i djelotvornost lijeka Versatis u pacijenata mlađih od 18 godina nisu utvrđeni. Nema dostupnih podataka.
04.3 Kontraindikacije
Preosjetljivost na djelatnu tvar ili neku od pomoćnih tvari navedenih u dijelu 6.1. Flaster je također kontraindiciran u pacijenata s poznatom preosjetljivošću na druge lokalne anestetike amidnog tipa, poput bupivakaina, etidokaina, mepivakaina i prilokaina.
Flaster se ne smije stavljati na upaljenu ili oštećenu kožu, kao što su aktivne lezije herpes zostera, atopijski dermatitis, rane.
04.4 Posebna upozorenja i mjere opreza pri uporabi
Flaster se ne smije stavljati na sluznicu. Treba izbjegavati kontakt flastera s očima.
Flaster sadrži propilen glikol koji može izazvati iritaciju kože. Sadrži i metil parahidroksibenzoat i propil parahidroksibenzoat koji mogu izazvati alergijske reakcije (čak i odgođene).
Flaster se mora koristiti s oprezom u bolesnika s teškim oštećenjem srca, bubrega ili jetre.
Uočeno je da jedan od metabolita lidokaina, 2,6 ksilidin, ima genotoksični i kancerogeni učinak na štakorima (vidjeti dio 5.3). Pokazalo se da su sekundarni metaboliti mutageni. Klinički značaj ovog nalaza nije poznat. Slijedom toga, dugotrajno liječenje lijekom Versatis opravdano je samo stvarnom terapijskom koristi za pacijenta (vidjeti dio 4.2).
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija
Do sada nisu dostupne studije interakcija. U kliničkim ispitivanjima s flasterom nisu zabilježene klinički relevantne interakcije.
Budući da su najveće koncentracije lidokaina u plazmi zabilježene u kliničkim ispitivanjima s flasterom niske (vidjeti dio 5.2), klinički značajne farmakokinetičke interakcije su malo vjerojatne.
Iako je obično apsorpcija lidokaina kroz kožu niska, flaster treba koristiti s oprezom u bolesnika koji primaju antiaritmike klase I (npr. Tokainid, meksiletin) ili druge lokalne anestetike, jer se ne može isključiti rizik od učinka sustavnog dodatka.
04.6 Trudnoća i dojenje
Trudnoća
Lidokain prolazi placentnu barijeru. Međutim, nema dovoljno podataka o uporabi lidokaina u trudnica.
Studije na životinjama ne ukazuju na teratogeni potencijal lidokaina. (vidi točku 5.3.).
Potencijalni rizik za ljude je nepoznat pa se Versatis ne smije koristiti tijekom trudnoće, osim ako je jasno naznačeno.
Dojenje
Lidokain se izlučuje u majčino mlijeko. Međutim, za flaster nema kliničkih studija na dojiljama. Budući da je metabolizam lidokaina relativno brz i javlja se gotovo potpuno u jetri, pretpostavlja se da se samo vrlo mala količina lidokaina može izlučiti u majčino mlijeko.
Plodnost
Nema dostupnih kliničkih podataka o plodnosti. Studije na životinjama nisu pokazale utjecaj na plodnost žena.
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima
Nisu provedena ispitivanja utjecaja na sposobnost upravljanja vozilima i rada sa strojevima. Budući da je sustavna apsorpcija minimalna (dio 5.2), učinci na sposobnost upravljanja vozilima i rada sa strojevima nisu vjerojatni.
04.8 Nuspojave
Sljedeći neželjeni učinci prijavljeni su prema padajućem redoslijedu ozbiljnosti unutar svake skupine učestalosti.
Otprilike 16% pacijenata koji se liječe mogu osjetiti nuspojave. To su lokalne reakcije zbog karakteristika lijeka.
Najčešće prijavljene nuspojave bile su reakcije na mjestu primjene (poput peckanja, dermatitisa, eritema, pruritusa, osipa, iritacije kože i mjehurića).
U donjoj tablici navedene su nuspojave prijavljene od pacijenata koji su koristili flaster u studijama postherpetične neuralgije. Navedeni su prema klasi i učestalosti u različitim uređajima. Njihova učestalost definirana je kao: vrlo česte ≥ 1/10; česte ≥ 1/100 do
Sljedeće reakcije primijećene su u pacijenata koji su koristili flaster u postmarketinškom okruženju
Sve nuspojave bile su općenito blage ili umjerene jačine. Manje od 5% njih dovelo je do prekida liječenja.
Uz odgovarajuću uporabu flastera, sustavne nuspojave su malo vjerojatne jer je sistemska koncentracija lidokaina vrlo niska (vidjeti dio 5.2). Sistemske nuspojave lidokaina slične su onima primijećenim za druge amide koji se koriste kao lokalni anestetici (vidjeti dio 4.9).
Prijavljivanje sumnji na nuspojave
Izvještavanje o sumnjama na nuspojave koje se jave nakon odobrenja lijeka važno je jer omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih djelatnika se traži da prijave sve sumnje na nuspojave putem nacionalnog sustava za prijavu. "Talijanska agencija za lijekove Web stranica: http://www.agenziafarmaco.gov.it/it/responsabili
04.9 Predoziranje
Predoziranje flasterom nije vjerojatno, ali se ne može isključiti da neprimjerena upotreba flastera, poput istodobne uporabe velikog broja flastera, na dulje razdoblje primjene ili upotrebe na slomljenoj koži, može dovesti do veće od normalne plazme razine lidokaina. Mogući znakovi sustavne toksičnosti slične su prirode onima koji se vide nakon primjene lidokaina kao lokalnog anestetika i mogu uključivati sljedeće znakove i simptome: omaglicu, povraćanje, somnolenciju, napadaje, midrijazu, bradikardiju, aritmiju i šok.
Nadalje, poznate interakcije između sustavnih koncentracija lidokaina s beta-blokatorima, inhibitorima CYP3A4 (npr. Derivati imidazola, makrolidi) i antiaritmičkim lijekovima mogu postati relevantne u slučaju predoziranja.
Ako se sumnja na predoziranje, flaster treba ukloniti i poduzeti mjere podrške ako je klinički potrebno. Ne postoji protuotrov za lidokain.
05.0 FARMAKOLOŠKA SVOJSTVA
05.1 Farmakodinamička svojstva
Farmakoterapijska skupina: lokalni anestetici, amidi
ATC oznaka: N01BB02
Mehanizam djelovanja
Versatis ima dvostruki mehanizam djelovanja: farmakološko djelovanje lidokaina i mehaničko djelovanje hidrogelnog flastera koji štiti preosjetljivo područje.
Lidokain koji se nalazi u flasterima Versatis neprestano se širi u kožu pružajući lokalni analgetski učinak. Mehanizam djelovanja povezan je sa stabilizacijom neuronskih membrana, za koju se vjeruje da određuje jednu dolje regulacija natrijevih kanala, a time i smanjenje boli.
Klinička učinkovitost
Liječenje boli u NPH -u je teško. Postoje dokazi o učinkovitosti Versatisa u simptomatskom ublažavanju alodinamičke komponente NPH -a u nekim slučajevima (vidjeti dio 4.2).
Učinkovitost lijeka Versatis dokazana je u studijama o postherpetičnoj neuralgiji.
Provedene su dvije glavne kontrolirane studije za procjenu učinkovitosti 5% flastera liječenih lidokainom.
U prvoj studiji pacijenti su bili regrutirani iz prethodno vjerovane populacije "odgovorilacTo je bila unakrsna studija koja je uključivala 14 dana liječenja s 5% lijekova s lidokainom, nakon čega je slijedilo placebo ili obrnuto. Primarni cilj bio je "vrijeme za izlaz", to jest, kad su pacijenti napustili studiju jer je ublažavanje boli bilo 2 boda niže od njihovog uobičajenog odgovora na ljestvici od 6 točaka (od pogoršanja do potpunog ublažavanja boli). Od 32 angažirana pacijenta, 30 je završilo studiju. The "vrijeme za izlaz" Prosječna vrijednost za placebo bila je 4 dana, dok je za aktivni lijek bila 14 dana (str
U drugoj studiji, 265 pacijenata s postherpetičnom neuralgijom regrutirano je na 8-tjedni otvoreni tretman s 5% gipsa ljekovitim lidokainom. U ovoj nekontroliranoj studiji, otprilike 50% pacijenata odgovorilo je na liječenje smanjenjem od najmanje četiri boda na ljestvici od 6 točaka (od pogoršanja do potpunog olakšanja). Ukupno je 71 pacijent randomiziran da prima placebo ili 5% lijekove s lidokainom koji su primijenjeni 2-14 dana. Primarna krajnja točka definirana je kao nedostatak učinkovitosti tijekom 2 uzastopna dana jer je ublažavanje boli bilo dva boda niže od normalnog odgovora na ljestvici od šest točaka (u rasponu od pogoršanja do potpune remisije) što je dovelo do prekida liječenja. Do prekida je došlo zbog neučinkovitosti u 9/36 pacijenata liječenih lijekom i u 16/35 pacijenata liječenih placebom.
Post-hoc analize druge studije pokazale su da je početni odgovor bio neovisan o trajanju već postojećeg stanja NPH. Međutim, činjenica da pacijenti s duljim trajanjem NPH (> 12 mjeseci) imaju najveću korist od aktivnog liječenja potkrijepljen je nalazom da je ova skupina pacijenata češće odustajala od ispitivanja zbog neučinkovitosti pri prelasku na placebo liječenje tijekom dvostruko slijepe faze studija.
U otvorenoj kontroliranoj studiji čini se da Versatis ima "usporedivu učinkovitost s pregabalinom u 98 pacijenata s PHN-om, s povoljnim sigurnosnim profilom.
05.2 "Farmakokinetička svojstva
Apsorpcija
Kad se 5% -tni lijek s lidokainom koristi u preporučenoj maksimalnoj dozi (3 flastera istovremeno nanesena tijekom 12 sati), približno 3 ± 2% ukupne primijenjene doze lidokaina je sistemski dostupno za jednokratnu i višestruku primjenu.
Populacijska kinetička analiza provedena tijekom kliničkih studija učinkovitosti kod pacijenata s NPH pokazala je srednju maksimalnu koncentraciju lidokaina od 45 ng / ml nakon istovremene primjene 3 flastera, 12 sati dnevno, ponavljanih do godinu dana. Ova se vrijednost slaže s onom utvrđenom u farmakokinetičkim studijama u bolesnika s NPH (52 ng / mL) i u zdravih dobrovoljaca (85 ng / mL i 125 ng / mL).
Nije bilo tendencije nakupljanja lidokaina i njegovih metabolita MEGX, GX i 2,6 ksilidina; koncentracije pri stacionarno stanje dostižu se u prva 4 dana.
Kinetička analiza stanovništva pokazala je da sustavna izloženost pokazuje proporcionalno manji porast od broja istodobno primijenjenih flastera, kada se njihov broj poveća s 1 na 3.
Distribucija
Nakon intravenozne primjene lidokaina zdravim dobrovoljcima, volumen distribucije bio je 1,3 ± 0,4 L / kg (srednja vrijednost ± S.D., n = 15). Volumen distribucije ne ovisi o dobi, smanjen je u bolesnika sa kongestivnom srčanom bolešću i povećan u bolesnika s bolestima jetre. Pri koncentracijama u plazmi utvrđenim primjenom flastera, približno 70% lidokaina veže se na proteine plazme.Lidokain prelazi placentnu i krvno-moždanu barijeru vjerojatno pasivnom difuzijom.
Biotransformacija
Lidokain se brzo metabolizira u jetri u niz metabolita. Glavni metabolički put lidokaina je N-dealkilacija u monoetilglicinksilidid (MEGX) i glicinksilidid (GX), oba su manje aktivna od lidokaina i dostupna su u niskim koncentracijama. Ti se metaboliti hidroliziraju u 2,6-ksilidin koji se konjugacijom pretvara u 4-hidroksi-2,6-ksilidin.
Farmakološka aktivnost metabolita 2,6-ksilidina nije poznata, ali pokazuje kancerogeni potencijal kod štakora (vidjeti dio 5.3.) Kinetička analiza populacije otkrila je srednju maksimalnu koncentraciju 2,6-ksilidina od 9 ng / ml nakon ponavljanja dnevno prijave do 1 godine. Ovaj nalaz potvrđuje farmakokinetička studija faze I. Podaci o metabolizmu lidokaina u koži nisu dostupni.
Uklanjanje
Lidokain i njegovi metaboliti izlučuju se bubrezima. Više od 85% doze se izlučuje urinom u obliku metabolita ili aktivne tvari. Manje od 10% doze lidokaina izlučuje se nepromijenjeno. Glavni metabolit u urinu je konjugat 4-hidroksi-2, 6-ksilidin., Što predstavlja otprilike 70-80% doze izlučene urinom. U ljudi se 2,6-ksilidin izlučuje urinom u koncentracijama ispod 1% doze. Srednji poluvijek eliminacije lidokaina nakon primjene flastera u zdravih dobrovoljaca je 7,6 sati. Izlučivanje lidokaina i njegovih metabolita može biti odgođeno u slučaju srčane, bubrežne ili jetrene insuficijencije.
05.3 Pretklinički podaci o sigurnosti
Učinci u pretkliničkim studijama opće toksičnosti opaženi su samo u dozama za koje se smatra da su dovoljno veće od najveće moguće izloženosti ljudi, što ukazuje na nisku kliničku važnost.
Lidokain hidroklorid u studijama nije bio genotoksičan in vitro ili in vivo. Njegov metabolit proizveden hidrolizom, 2,6-ksilidin, pokazao je genotoksično djelovanje u nekoliko testova, osobito nakon metaboličke aktivacije.
Studije karcinogenosti s lidokainom nisu provedene. Studije provedene na metabolitu 2,6-ksilidinu, pomiješanom u prehrani mužjaka i ženki štakora, pokazale su citotoksičnost povezanu s liječenjem: uočena je i hiperplazija mirisnog epitela nosa, karcinomi i adenomi u nosnim šupljinama. na razini jetre i potkožno. Budući da je rizik za ljude nejasan, treba izbjegavati dugotrajno liječenje lidokainom.
Lidokain nije imao utjecaja na ukupnu reproduktivnu sposobnost, plodnost ženki ili embriofetalni razvoj / teratogenezu u štakora podvrgnutih koncentracijama u plazmi do 50 puta većim od onih zabilježenih u bolesnika. Studije na životinjama u vezi s plodnošću muškaraca, porođajem ili postnatalnim razvojem nisu potpune.
06.0 FARMACEUTSKI PODACI
06.1 Pomoćne tvari
Samoljepljivi sloj
Glicerol, sorbitol koji se može kristalizirati, natrij karmeloza, propilen glikol (E1520), urea, teški kaolin, vinska kiselina, želatina, polivinil alkohol, aluminij glicinat, dinatrijev edetat, metil parahidroksibenzoat (E218), propil parahidroksibenzoat (E216), poliakril kiselina, poliakrilat, pročišćena voda.
Podrška
Polietilen tereftalat (PET)
Film
Polietilen tereftalat
06.2 Nekompatibilnost
Nije bitno.
06.3 Razdoblje valjanosti
3 godine.
Nakon otvaranja vrećice, flaster se mora upotrijebiti u roku od 14 dana.
06.4 Posebne mjere pri skladištenju
Nemojte hladiti ili zamrzavati. Vrećicu držite zatvorenom nakon prvog otvaranja.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja
Vreće za ponovno zatvaranje izrađene od metaakrilnog ko-polimera od papira / polietilena / aluminija / etilenske kiseline, koje sadrže 5 zakrpa.
Svako pakiranje sadrži 5, 10, 20, 25 ili 30 flastera.
Ne mogu se na tržište staviti sve veličine pakiranja.
06.6 Upute za uporabu i rukovanje
Nakon upotrebe flaster i dalje sadrži aktivni sastojak. Nakon uklanjanja flaster treba presaviti na pola, s ljepljivim slojem prema unutra, tako da samoljepljivi sloj nije izložen i mora se odbaciti.
Neiskorišteni ili odbačeni flaster treba zbrinuti u skladu s lokalnim propisima.
07.0 Nositelj odobrenja za stavljanje u promet
DRŽAČ AIC -a: GRÜNENTHAL ITALIA S.r.l. putem Carlo Bo 11 20143 Milan
08.0 BROJ DOZVOLE ZA PROMET
10 ljekovitih flastera 5% AIC n. 040335022
30 ljekovitih flastera 5% AIC n. 040335059
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA
Datum prve registracije: ožujak 2012
Datum posljednje obnove: 5.01.2012
10.0 DATUM REVIZIJE TEKSTA
30. svibnja 2015













.jpg)