Aktivni sastojci: Famciklovir
Famvir 125 mg filmom obložene tablete
Famvir 250 mg filmom obložene tablete
Famvir 500 mg filmom obložene tablete
Zašto se koristi Famvir? Čemu služi?
Famvir je antivirusni lijek. Sprječava reprodukciju zaraženog virusa. Budući da se virus brzo razmnožava kad infekcija počne, dobit ćete bolje rezultate ako uzmete Famvir čim se pojave prvi simptomi.
Famvir se koristi za liječenje dvije vrste virusnih infekcija kod odraslih:
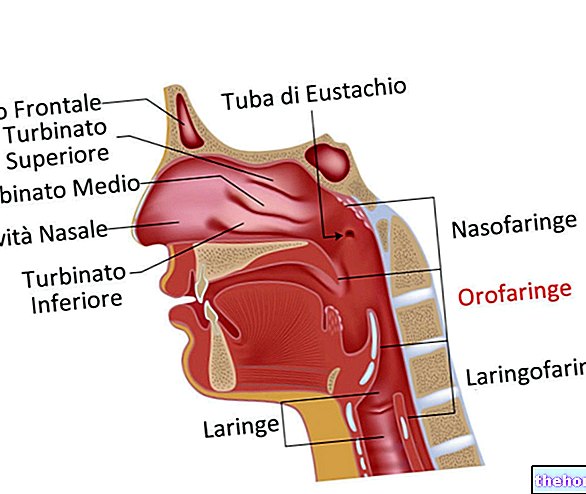
- Herpes zoster, virusna infekcija uzrokovana virusom koji se naziva varicella zoster (isti virus koji uzrokuje vodene kozice). Famvir sprječava širenje virusa u tijelu pa do ozdravljenja može doći brže.
- Famvir se također koristi za liječenje infekcija u području oko oka ili čak u samom oku (oftalmološki zoster).
- Genitalnog herpesa. Genitalni herpes je virusna infekcija uzrokovana virusom herpes simplex tipa 1 ili 2. Obično se prenosi spolno. Izaziva žuljeve i pečenje ili svrbež genitalija, što može biti bolno. Famvir se koristi za liječenje herpes infekcija. Genitalni kod odraslih Ljudi koji imaju česte epizode genitalnog herpesa također mogu uzeti Famvir kako bi pokušali spriječiti nove epizode.
Kontraindikacije Kada se Famvir ne smije koristiti
Nemojte uzimati Famvir
- Ako ste alergični na famciklovir, bilo koji drugi sastojak ovog lijeka (naveden u odjeljku 6) ili penciklovir (aktivni metabolit famciklovira i komponenta nekih drugih lijekova).
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Famvir
Pitajte svog liječnika za savjet ako mislite da ste alergični.
Upozorenja i mjere opreza
Prije uzimanja Famvira razgovarajte sa svojim liječnikom
- Ako imate problema s bubrezima (ili ste ih imali u prošlosti). Vaš liječnik može odlučiti propisati nižu dozu Famvira.
- Ako imate poremećaje imunološkog sustava.
- Ako imate problema s jetrom.
Ako se bilo što od navedenog odnosi na vas, obratite se svom liječniku prije nego uzmete Famvir
Djeca i adolescenti (mlađi od 18 godina): Famvir se ne preporučuje za primjenu u djece i adolescenata.
Sprječavanje prijenosa genitalnog herpesa na druge osobe
Ako uzimate Famvir za liječenje ili suzbijanje genitalnog herpesa, ili ako ste u prošlosti patili od genitalnog herpesa, trebali biste nastaviti imati siguran spolni odnos pomoću kondoma. Ovo je važno kako bi se spriječio prijenos infekcije na druge osobe.. Ne biste trebali imati spolne odnose ako imate genitalne mjehuriće.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak Famvira
Obavijestite svog liječnika ili ljekarnika ako uzimate, nedavno ste uzimali ili biste mogli uzeti bilo koje druge lijekove, uključujući i lijekove koji se mogu nabaviti bez recepta.
Posebno je važno da obavijestite svog liječnika ili ljekarnika ako uzimate neki od sljedećih lijekova:
- Raloksifen (koristi se za sprječavanje i liječenje osteoporoze).
- Probenecid (koristi se za liječenje visoke razine mokraćne kiseline u krvi povezane s gihtom i za povećanje razine antibiotika sličnih penicilinu u krvi) ili bilo koji drugi lijek koji može oštetiti bubrege.
Famvir uz hranu i piće
Famvir se može uzimati sa ili bez hrane
Upozorenja Važno je znati da:
Trudnoća, dojenje i plodnost
Ako ste trudni ili dojite, mislite da ste trudni ili planirate trudnoću, pitajte svog liječnika za savjet prije nego uzmete ovaj lijek. Famvir se ne smije koristiti tijekom trudnoće osim ako je to nužno potrebno. Vaš će liječnik razgovarati s vama o potencijalnim rizicima uzimanja Famvira tijekom trudnoće.
Famvir se ne smije koristiti tijekom dojenja osim ako je to apsolutno neophodno. Vaš liječnik će s vama razgovarati o mogućim rizicima uzimanja Famvira tijekom dojenja.
Upravljanje vozilima i strojevima
Famvir može uzrokovati omaglicu, pospanost ili zbunjenost. Nemojte voziti niti upravljati strojevima ako primijetite bilo koji od ovih simptoma tijekom uzimanja Famvira
Famvir 125 mg filmom obložene tablete sadrže laktozu
Ako vam je liječnik rekao da ne podnosite neke šećere, poput laktoze, obratite se svom liječniku prije uzimanja ovog lijeka.
Famvir 250 mg filmom obložene tablete sadrže laktozu
Ako vam je liječnik rekao da ne podnosite neke šećere, poput laktoze, obratite se svom liječniku prije uzimanja ovog lijeka.
Doza, način i vrijeme primjene Kako se koristi Famvir: Doziranje
Uvijek uzimajte ovaj lijek točno onako kako vam je rekao liječnik. Ako ste u nedoumici, obratite se svom liječniku ili ljekarniku.
- Dnevna doza i trajanje liječenja ovisit će o vrsti virusne infekcije koju imate - pogledajte dolje. Vaš liječnik će vam propisati ispravnu dozu.
- Za najbolje rezultate počnite uzimati lijek što je prije moguće nakon pojave prvih znakova i simptoma.
- Izbjegavajte spolni kontakt ako osjetite simptome genitalnog herpesa - čak i ako ste već započeli liječenje Famvirom. To je zato što bi mogao prenijeti infekciju na vašeg partnera
- Ako imate ili ste imali problema s bubrezima, liječnik će vam možda odlučiti dati manju dozu Famvira.
Doza za herpes zoster
Ako imate normalan imunološki sustav, preporučena doza je
- 500 mg tri puta dnevno, sedam dana
Ako je vaša imunološka obrana smanjena, preporučena doza je
- 500 mg tri puta dnevno, deset dana
Doza za genitalni herpes
Doza ovisi o stanju vašeg imunološkog sustava i stadiju infekcije.
Ako imate normalan imunološki sustav, doze su sljedeće:
Za prvi osip preporučena doza je:
- 250 mg tri puta dnevno, pet dana.
Za liječenje daljnjih osipa, preporučena doza je:
- 125 mg dva puta dnevno, pet dana.
Za prevenciju budućih osipa, preporučena doza je:
- 250 mg dva puta dnevno.
Vaš liječnik će vam reći koliko dugo trebate nastaviti uzimati tablete.
Ako je vaša imunološka obrana niska, doze su sljedeće:
Za liječenje tekućeg osipa, preporučena doza je:
- 500 mg dva puta dnevno, sedam dana.
Za prevenciju budućih osipa, doza je:
- 500 mg dva puta dnevno.
Vaš liječnik će vam reći koliko dugo trebate nastaviti uzimati tablete.
Ako ste zaboravili uzeti Famvir
Ako ste zaboravili uzeti dozu Famvira, trebali biste je uzeti čim se sjetite. Zatim uzmite sljedeću dozu prema planu. Međutim, nemojte uzeti dvije doze u manje od 1 sata: u tom slučaju trebate preskočiti propuštenu dozu. Također nemojte uzeti dvostruku dozu kako biste nadoknadili zaboravljenu dozu.
Ako imate dodatnih pitanja o uporabi ovog lijeka, obratite se svom liječniku ili ljekarniku.
Predoziranje Što učiniti ako ste uzeli previše Famvira
Ako ste uzeli više tableta nego što vam je rečeno ili ako je netko drugi slučajno uzeo vaš lijek, odmah se obratite svom liječniku ili bolnici. Pokažite im svoju kutiju tableta.
Uzimanje previše Famvira može utjecati na bubrege. U pacijenata koji već imaju bubrežnih problema, ako se doze ne smanje na odgovarajući način, to rijetko može dovesti do zatajenja bubrega.
Nuspojave Koje su nuspojave Famvira
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih.
Ozbiljne nuspojave Famvira su:
Većina ovih nuspojava su rijetke ili rijetke (javljaju se kod 1 do 100 od 10.000 pacijenata).
- Teški osip s mjehurićima na koži ili sluznici usana, očiju, usta, nosnih prolaza ili genitalija (to mogu biti znakovi teške alergijske kožne reakcije).
- Modrice bez objašnjivog uzroka, crvenkaste ili ljubičaste mrlje na koži ili krvarenje iz nosa (to mogu biti znakovi smanjenja broja trombocita).
- Oticanje ispod površine kože (npr. Oticanje lica, oticanje oko oka, oticanje kapka, oticanje grla).
- Žuta promjena boje kože i / ili očiju (znakovi žutice).
- Ljubičaste mrlje na koži, svrbež, peckanje (znakovi upale krvnih žila).
Obratite se liječniku ili idite u hitnu službu najbliže bolnice ako osjetite bilo koju od ovih nuspojava.
Vrlo česte nuspojave (ove se nuspojave javljaju u više od 1 na 10 osoba)
- Glavobolja
Česte nuspojave (ove se nuspojave javljaju u do 1 na 10 osoba)
- Mučnina (mučnina)
- Povukao se
- Bol u trbuhu
- Proljev
- Vrtoglavica
- Osip
- Svrab
- Abnormalne vrijednosti u testovima funkcije jetre
Manje česte nuspojave (ove se nuspojave javljaju u do 1 na 100 osoba)
- Zbunjenost
- Somnolencija (obično u starijih osoba)
- Svrbež (osip)
Rijetke nuspojave (ove se nuspojave javljaju u do 1 na 1000 osoba)
- Halucinacije (vidjeti ili čuti stvari kojih zapravo nema)
- Palpitacije (znakovi abnormalnog rada srca)
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku ili ljekarniku.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Također možete prijaviti nuspojave izravno putem nacionalnog sustava prijavljivanja na "www.agenziafarmaco.it/it/responsabili". Prijavljivanjem nuspojava možete pomoći u pružanju više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
- Čuvajte ovaj lijek izvan pogleda i dohvata djece.
- Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na naljepnici iza Rok valjanosti: Rok valjanosti odnosi se na zadnji dan tog mjeseca.
- Ne čuvati na temperaturi iznad 25 ° C.
- Čuvati u originalnom pakiranju radi zaštite od vlage.
- Nemojte koristiti ovaj lijek ako primijetite da je pakiranje oštećeno ili pokazuje znakove neovlaštenog rukovanja.
- Nemojte bacati lijekove u otpadne vode ili kućni otpad. Pitajte ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Druge podatke
Što Famvir sadrži
Famvir 125 mg filmom obložene tablete
- Aktivni sastojak je famciklovir.
- Pomoćni sastojci su bezvodna laktoza, natrijev škrob glikolat (tip A), hidroksipropilceluloza i magnezijev stearat. Obloga tablete sastoji se od hipromeloze, titanijevog dioksida (E171), Macrogola 4000 i Macrogola 6000.
Famvir 250 mg filmom obložene tablete
- Aktivni sastojak je famciklovir.
- Pomoćni sastojci su bezvodna laktoza, natrijev škrob glikolat (tip A), hidroksipropilceluloza i magnezijev stearat. Obloga tablete sastoji se od hipromeloze, titanijevog dioksida (E171), Macrogola 4000 i Macrogola 6000.
Famvir 500 mg filmom obložene tablete
- Aktivni sastojak je famciklovir.
- Pomoćni sastojci su natrijev škrobni glikolat (tip A), hidroksipropilceluloza i magnezijev stearat. Obloga tablete sastoji se od hipromeloze, titanijevog dioksida (E171), Macrogola 4000 i Macrogola 6000.
Izgled Famvira i sadržaj pakiranja
Famvir je dostupan u obliku filmom obloženih tableta.
Famvir 125 mg filmom obložene tablete
Bijela, okrugla, bikonveksna filmom obložena tableta sa zakošenim rubovima, utisnuta s "FV" na jednoj strani i "125" na drugoj.
Famvir 250 mg filmom obložene tablete
Bijela, okrugla, bikonveksna filmom obložena tableta sa zakošenim rubovima, utisnuta s "FV" na jednoj strani i "250" na drugoj.
Famvir 500 mg filmom obložene tablete
Bijela, ovalna, bikonveksna filmom obložena tableta sa zakošenim rubovima, s ugraviranim natpisom "FV 500" samo na jednoj strani.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA
FAMVIR
02.0 KVALITATIVNI I KOLIČINSKI SASTAV
Svaka filmom obložena tableta sadrži 125 mg, 250 mg ili 500 mg famciklovira.
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK
Filmom obložena tableta.
04.0 KLINIČKI PODACI
04.1 Terapeutske indikacije
Infekcije virusom varicella -zoster (VZV) - herpes zoster
Famvir je indiciran za:
- liječenje herpes zostera i oftalmološkog zostera u imunokompetentnih odraslih osoba (vidjeti dio 4.4)
- liječenje herpes zostera u odraslih osoba s oslabljenim imunitetom (vidjeti dio 4.4.)
Infekcije virusom herpes simplex (HSV) - genitalni herpes
Famvir je indiciran za:
- liječenje prvih i ponavljajućih epizoda genitalnog herpesa u imunokompetentnih odraslih osoba
- liječenje ponavljajućih epizoda genitalnog herpesa u odraslih osoba s oslabljenim imunitetom
- suzbijanje ponavljajućeg genitalnog herpesa u imunokompetentnih i imunokompromitiranih odraslih osoba
Nisu provedena klinička ispitivanja na imunokompromitiranim pacijentima s HSV -om koji su uzrokovani osim HIV infekcijama (vidjeti dio 5.1).
04.2 Doziranje i način primjene
Herpes zoster u imunokompetentnih odraslih osoba
500 mg tri puta dnevno tijekom sedam dana za akutno liječenje oftalmološkog zostera.
Liječenje treba započeti što je prije moguće nakon dijagnoze šindre.
Herpes zoster u imunokompromitiranih odraslih osoba
500 mg tri puta dnevno deset dana.
Liječenje treba započeti što je prije moguće nakon dijagnoze šindre.
Genitalni herpes u imunokompetentnih odraslih osoba
Prva epizoda genitalnog herpesa: 250 mg tri puta dnevno tijekom pet dana. Preporuča se započeti liječenje što je prije moguće nakon dijagnoze prve epizode genitalnog herpesa.
Epizodično liječenje ponavljanog genitalnog herpesa: 125 mg dva puta dnevno tijekom pet dana. Preporuča se započeti liječenje što je prije moguće nakon pojave prodromalnih simptoma (npr. Trnci, svrbež, pečenje, bol) ili lezija.
Rekurentni genitalni herpes u imunokompromitiranih odraslih osoba
Epizodično liječenje ponavljanog genitalnog herpesa: 500 mg dva puta dnevno tijekom sedam dana. Preporuča se započeti liječenje što je prije moguće nakon pojave prodromalnih simptoma (npr. Trnci, svrbež, pečenje, bol) ili lezija.
Suzbijanje ponavljajućeg genitalnog herpesa u imunokompetentnih odraslih osoba
250 mg dva puta dnevno. Supresivnu terapiju treba prekinuti nakon najviše 12 mjeseci kontinuiranog antivirusnog liječenja kako bi se ponovno procijenila učestalost i ozbiljnost recidiva. Minimalno razdoblje revalorizacije mora uključivati dva ponavljanja. Pacijenti koji i dalje imaju značajnu bolest mogu ponovno započeti supresivno liječenje.
Suzbijanje ponavljajućeg genitalnog herpesa u imunokompromitiranih odraslih osoba
500 mg dva puta dnevno.
Pacijenti s oštećenom funkcijom bubrega
Budući da je smanjeni klirens penciklovira povezan sa smanjenom bubrežnom funkcijom, mjereno klirensom kreatinina, posebnu pozornost treba posvetiti doziranju u bolesnika s oštećenom bubrežnom funkcijom. Preporučene doze u odraslih bolesnika s oštećenjem bubrega prikazane su u tablici 1.
Tablica 1 Preporučene doze u odraslih bolesnika s oštećenom funkcijom bubrega
Bolesnici s oštećenjem bubrega na hemodijalizi
Budući da je četverosatna hemodijaliza rezultirala smanjenjem koncentracije penciklovira u plazmi do 75%, famciklovir treba primijeniti odmah nakon dijalize. Preporučene doze za bolesnike na hemodijalizi prikazane su u tablici 1.
Pacijenti s oštećenom funkcijom jetre
Nije potrebna prilagodba doze u bolesnika s blagim do umjerenim oštećenjem jetre. Nema podataka o bolesnicima s teškim oštećenjem jetre (vidjeti dijelove 4.4 i 5.2).
Stariji pacijenti (≥ 65 godina)
Nisu potrebne prilagodbe doze, osim u slučajevima oštećenja bubrežne funkcije.
Pedijatrijska populacija
Sigurnost i djelotvornost famciklovira u djece i adolescenata mlađih od 18 godina nisu utvrđeni.Trenutno dostupni podaci opisani su u odjeljcima 5.1 i 5.2.
Način primjene
Famvir se može uzimati s obrokom ili bez njega (vidjeti dio 5.2).
04.3 Kontraindikacije
Preosjetljivost na djelatnu tvar ili bilo koju pomoćnu tvar.
Preosjetljivost na penciklovir.
04.4 Posebna upozorenja i mjere opreza pri uporabi
Primjena u bolesnika s oštećenjem bubrega
U bolesnika s oštećenom bubrežnom funkcijom potrebno je prilagoditi dozu (vidjeti dijelove 4.2 i 4.9).
Primjena u bolesnika s oštećenjem jetre
Famciklovir nije ispitivan u bolesnika s teškim oštećenjem jetre. U tih se bolesnika može poremetiti transformacija famciklovira u njegov aktivni metabolit penciklovir, što rezultira nižim koncentracijama penciklovira u plazmi; stoga se može dogoditi smanjenje učinkovitosti famciklovira.
Koristi se za liječenje herpes zostera
Klinički odgovor mora se pažljivo pratiti, osobito u imunološki oslabljenih pacijenata. Kada se odgovor na oralnu terapiju smatra nedovoljnim, treba razmotriti intravenoznu antivirusnu terapiju.
Bolesnike sa kompliciranim herpes zosterom, tj. One s zahvaćenim visceralima, diseminiranim zosterom, motoričkim neuropatijama, encefalitisom i cerebrovaskularnim komplikacijama treba liječiti intravenoznom antivirusnom terapijom.
Osim toga, imunokompromitirane bolesnike s oftalmološkim zosterom ili one s visokim rizikom od širenja bolesti i zahvaćenosti visceralnih organa treba liječiti intravenoznom antivirusnom terapijom.
Prijenos genitalnog herpesa
Pacijente treba savjetovati da izbjegavaju spolne odnose ako su prisutni simptomi, čak i ako je započeto liječenje antivirusnim lijekovima. Tijekom supresivne terapije antivirusnim lijekovima, učestalost širenja virusa je značajno smanjena. Međutim, prijenos je i dalje moguć. Stoga se bolesnicima preporučuje uzimanje drugih mjera tijekom spolnog odnosa, uz terapiju famciklovirom.
Ostalo
Famvir 125 mg i 250 mg tablete sadrže laktozu. Bolesnici s rijetkim nasljednim oblicima intolerancije na galaktozu, nedostatkom Lapp laktaze ili sindromom malapsorpcije glukoze-galaktoze ne smiju uzimati ovaj lijek..
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija
Učinci drugih lijekova na famciklovir
Nisu identificirane klinički značajne interakcije.
Istodobna primjena probenecida može uzrokovati povećanje koncentracije penciklovira, aktivnog metabolita famciklovira u plazmi, zbog konkurencije u eliminaciji.
Stoga je potrebno nadzirati toksičnost bolesnika koji primaju famciklovir u dozi od 500 mg tri puta dnevno, istodobno s probenecidom. Ako pacijenti dožive jaku omaglicu, somnolenciju, zbunjenost ili druge smetnje središnjeg živčanog sustava, može se razmotriti smanjenje doze famciklovira na 250 mg tri puta dnevno.
Famciklovir zahtijeva da se enzim aldehid oksidaza pretvori u njegov aktivni metabolit penciklovir. Raloksifen se pokazao kao snažan inhibitor ovog enzima. in vitro. Istodobna primjena raloksifena mogla bi utjecati na stvaranje penciklovira, a time i na učinkovitost famciklovira. Kada se raloksifen primjenjuje s famciklovirom, potrebno je pratiti kliničku učinkovitost antivirusne terapije.
04.6 Trudnoća i dojenje
Trudnoća
Postoje ograničeni podaci (manje od 300 epizoda trudnoće) o uporabi famciklovira u trudnica. Na temelju ovih ograničenih podataka kumulativna analiza potencijalne i retrospektivne trudnoće nije dala dokaze da lijek uzrokuje specifične promjene fetusa ili urođene anomalije . Studije na životinjama nisu pokazale embriotoksične ili teratogene učinke na famciklovir ili penciklovir (aktivni metabolit famciklovira). Famciklovir se smije koristiti u trudnoći samo ako potencijalne koristi nadmašuju potencijalne rizike.
Vrijeme za hranjenje
Nije poznato izlučuje li se famciklovir u majčino mlijeko. Studije na životinjama pokazale su izlučivanje penciklovira u majčino mlijeko. Ako stanje žene zahtijeva liječenje famciklovirom, može se razmotriti prekid dojenja.
Plodnost
Klinički podaci ne pokazuju utjecaj famciklovira na plodnost muškaraca nakon dugotrajnog liječenja oralnom dozom od 250 mg dvaput dnevno (vidjeti dio 5.3).
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima
Nisu provedena ispitivanja koja bi istraživala učinke na sposobnost upravljanja vozilima i rada sa strojevima. Međutim, pacijenti koji uzimaju Famvir i osjećaju omaglicu, pospanost, zbunjenost ili druge poremećaje središnjeg živčanog sustava trebali bi se suzdržati od upravljanja vozilima i rada sa strojevima.
04.8 Nuspojave
U kliničkim ispitivanjima zabilježeni su glavobolja i mučnina. Ovi učinci općenito su bili blagi ili umjereni po intenzitetu, a također su se javljali sa sličnom učestalošću u bolesnika koji su uzimali placebo. Sve ostale nuspojave uočene su iz marketinga.
Cjelokupni skup placebo ili aktivno kontroliranih kliničkih ispitivanja (n = 2326 u grupi Famvir) retrospektivno je analiziran kako bi se dobila klasifikacija učestalosti pojavljivanja dolje navedenih nuspojava. U donjoj tablici, procijenjena učestalost Nuspojave se temelje na svim spontanim izvješćima i slučajevima opisanim u literaturi koji su prijavljeni za Famvir od njegovog početka. Nuspojave (Tablica 2) navedene su prema učestalosti, prema sljedećoj konvenciji: vrlo česte (≥ 1/10); česte (≥ 1/100,
Tablica 2 Nuspojave
Sveukupno, nuspojave uočene u kliničkim ispitivanjima kod imunokompromitiranih pacijenata bile su usporedive s onima prijavljenim u imunokompetentnoj populaciji. Češće su prijavljivani mučnina, povraćanje i abnormalni testovi funkcije jetre, osobito pri visokim dozama.
04.9 Predoziranje
Slučajevi predoziranja famciklovirom su ograničeni. U slučaju predoziranja potrebno je uvesti odgovarajuću simptomatsku i potpornu terapiju. Akutno zatajenje bubrega rijetko je prijavljeno u bolesnika s latentnom bubrežnom bolešću u kojih doza famciklovira nije adekvatno smanjena, u odnosu na razinu bubrežne funkcije. Penciklovir se može dijalizirati; plazma koncentracija se smanjuje za približno 75% nakon 4 sata hemodijalize.
05.0 FARMAKOLOŠKA SVOJSTVA
05.1 Farmakodinamička svojstva
Farmakoterapijska skupina: Nukleozidi i nukleotidi, isključujući inhibitore reverzne transkriptaze, ATC oznaka: J05A B09
Mehanizam djelovanja
Famciklovir je oralni prolijek penciklovira. Famciklovir se brzo pretvara in vivo na penciklovir, koji ima aktivnost in vitro protiv virusa herpes simpleksa (HSV tipovi 1 i 2), varicella zoster virusa, Epstein-Barr virusa i citomegalovirusa.
Antivirusni učinak oralno primijenjenog famciklovira dokazan je na nekoliko životinjskih modela: ovaj učinak posljedica je pretvorbe in vivo na penciklovir. U stanicama zaraženim virusom, timidin kinaza (TK) fosforilira penciklovir u oblik monofosfata, koji se pak staničnim kinazama pretvara u penciklovir trifosfat. Ovaj trifosfat ostaje u zaraženim stanicama više od 12 sati i inhibira produženje lanca virusne DNA konkurentnom inhibicijom s deoksiguanozin trifosfatom za ugradnju u rastuću virusnu DNA, čime se blokira replikacija virusne DNA. U stanicama koje nisu zaražene virusom, koncentracija penciklovir trifosfata je na granici praga određivanja. Stoga je vjerojatnost toksičnosti za stanice domaćina sisavaca niska, a malo je vjerojatno da će terapijske koncentracije penciklovira dovesti do farmakoloških učinaka na neinficirane stanice.
Otpor
Kao i kod aciklovira, najčešći oblik rezistencije opažen u sojeva virusa Herpes simplex (HSV) bio je nedostatak u proizvodnji enzima timidin kinaze (TK). Prema pencikloviru.
Rezultati 11 međunarodnih kliničkih studija provedenih na imunokompetentnim ili imunokompromitiranim pacijentima liječenim penciklovirom (topikalne i intravenozne formulacije) ili famciklovirom, uključujući ona ispitivanja u kojima su pacijenti liječeni famciklovirom do 12 mjeseci, pokazali su ukupnu nisku učestalost virusnih izolata otpornih na penciklovir: 0,2% (2/913) u imunokompetentnih pacijenata i 2,1% (6/288) u imunokompromitiranih pacijenata. Rezistentni izolati uglavnom su otkriveni na početku terapije ili u placebo skupini, a rezistencija se pojavila tijekom ili nakon liječenja famciklovirom ili penciklovirom u samo dva imunološki oslabljena bolesnika.
Klinička učinkovitost
U placebo i aktivno kontroliranim studijama i kod imunokompetentnih i kod imunokompromitiranih pacijenata s nekompliciranim herpes zosterom, utvrđeno je da je famciklovir učinkovit u zacjeljivanju rana. U aktivnom kontroliranom kliničkom ispitivanju, famciklovir se pokazao učinkovitim u liječenju oftalmološkog zostera u imunokompetentnih pacijenata.
Učinkovitost famciklovira u imunokompetentnih bolesnika s prvom epizodom genitalnog herpesa dokazana je u tri aktivno kontrolirane studije. Dvije placebo kontrolirane studije u imunokompetentnih bolesnika i jedna aktivno kontrolirana studija u HIV-inficiranih pacijenata s ponovljenim genitalnim herpesom pokazale su da je famciklovir je djelotvoran.
Dvije 12-mjesečne placebo kontrolirane studije provedene na imunokompetentnim pacijentima s recidivirajućim genitalnim herpesom pokazale su da su bolesnici liječeni famciklovirom imali značajno smanjenje recidiva u odnosu na bolesnike liječene placebom. Placebo kontrolirane i nekontrolirane studije u trajanju do 16 tjedana pokazale su da je famciklovir učinkovit u suzbijanju ponavljanog genitalnog herpesa u pacijenata zaraženih HIV-om; placebom kontrolirana studija pokazala je da je famciklovir značajno smanjio udio dana simptomatskog i asimptomatskog širenja virusa herpes simpleksa.
Pedijatrijska populacija
Ispitna formulacija granule famciklovira za oralnu primjenu proučavana je u 169 pedijatrijskih pacijenata u dobi od 1 mjeseca do 12 godina. Stotina ovih pacijenata, u dobi od 1 do 12 godina, liječeno je oralnim granulama famciklovira (u dozama između 150 mg i 500 mg) dva puta dnevno (47 bolesnika s infekcijama herpes simpleksa) ili tri puta dnevno (53 bolesnika s varičelama) za 7 dana. Preostalih 69 pacijenata (18 pacijenata u dobi od 1 do 12 mjeseci, 51 bolesnik u dobi od 1 do 12 godina) sudjelovalo je u farmakokinetičkim i sigurnosnim studijama koristeći pojedinačne doze oralnih granula famciklovira (u dozama u rasponu od 25 mg i 500 mg). Doze famciklovira, temeljene na tjelesnoj težini, odabrane su kako bi se dobila slična "sustavna izloženost penciklovira" sistemskoj izloženosti pencikloviru primijećena kod odraslih osoba nakon primjene 500 mg famciklovira. Nijedna od ovih studija nije uključivala kontrolnu skupinu; stoga se ne može izvući zaključak o učinkovitosti proučavanih režima doziranja. Sigurnosni profil bio je sličan onomu koji je primijećen u odraslih. Međutim, sustavna izloženost lijeku bila je niska u djece mlađe od 6 mjeseci, čime je spriječena bilo kakva procjena sigurnosti famciklovir u ovoj populaciji.
05.2 Farmakokinetička svojstva
Osnovne značajke
Apsorpcija
Famciklovir je oralni prolijek penciklovira, aktivnog metabolita protiv virusa. Nakon oralne primjene, famciklovir se brzo i opsežno apsorbira i pretvara u penciklovir. Bioraspoloživost penciklovira nakon oralne primjene famciklovira bila je 77%. Najviša koncentracija penciklovira u plazmi nakon oralnih doza od 125 mg, 250 mg, 500 mg i 750 mg famciklovira bila je 0,8 mcg / ml, 1,6 mcg / ml, 3,3 mcg / ml, odnosno 5,1 mcg / ml, i postignuta je u srednjem vremenu od 45 minuta nakon primjene.
Krivulje koncentracije penciklovira u plazmi u odnosu na vrijeme slične su nakon jednokratne i ponovljene primjene (tri puta i dva puta dnevno), što ukazuje na to da nema nakupljanja penciklovira nakon ponovljene primjene famciklovira.
Hrana ne utječe na sustavnu dostupnost (AUC) oralno primijenjenog penciklovira izvedenog iz famciklovira.
Distribucija
Penciklovir i njegov 6-deoksi prekursor slabo su vezani za proteine plazme (manje od 20%).
Metabolizam i eliminacija
Famciklovir se izlučuje prvenstveno kao penciklovir i kao prekursor 6-deoksi, a oba se izlučuju urinom. Nema koncentracija nepromijenjenog famciklovira u urinu. Tubularna sekrecija doprinosi bubrežnoj eliminaciji penciklovira.
Poluvrijeme eliminacije penciklovira u plazmi nakon jednokratne i ponovljene primjene famciklovira bilo je približno 2 sata.
Rezultati pretkliničkih studija nisu pokazali potencijal za indukciju enzima citokroma P450 i inhibiciju CYP3A4.
Karakteristike u posebnim populacijama
Bolesnici s herpes zoster infekcijom
Nekomplicirana infekcija herpes zoster ne mijenja značajno farmakokinetiku penciklovira nakon oralne primjene famciklovira. Nakon jednokratne i ponovljene primjene famciklovira u bolesnika s herpes zosterom, terminalno poluvrijeme penciklovira u plazmi bilo je 2, odnosno 8, odnosno 2,7 sati.
Ispitanici s oštećenjem bubrega
Nakon primjene pojedinačnih i ponovljenih doza, prividni klirens plazme, bubrežni klirens i konstantna brzina eliminacije penciklovira u plazmi smanjivali su se proporcionalno smanjenju bubrežne funkcije. U bolesnika s oštećenjem bubrega potrebna je prilagodba doze (vidjeti dio 4.2).
Ispitanici s oštećenjem jetre
Blago i umjereno oštećenje jetre nije pokazalo utjecaj na sistemsku dostupnost penciklovira nakon oralne primjene famciklovira. Nije potrebna prilagodba doze u bolesnika s blagim do umjerenim oštećenjem jetre (vidjeti dijelove 4.2 i 4.4). Farmakokinetika penciklovira nije ispitivana u bolesnika s teškim oštećenjem jetre. U tih se bolesnika može poremetiti pretvorba famciklovira u aktivni metabolit penciklovir, što rezultira nižim koncentracijama penciklovira u plazmi, a time i mogućim smanjenjem učinkovitosti famciklovira.
Pedijatrijski bolesnici
Ponovljene oralne doze famciklovira (250 mg ili 500 mg tri puta dnevno) davane pedijatrijskim bolesnicima (od 6 do 11 godina) s infekcijom hepatitisom B nisu imale značajan učinak na farmakokinetiku penciklovira u usporedbi s onom postignutom pri jednokratnoj dozi. Nije došlo do nakupljanja penciklovira.
U djece (1-12 godina) s herpes simplex infekcijom ili s vodenim kozicama koje su uzimale pojedinačne doze famciklovira (vidjeti dio 5.1), prividni klirens penciklovira povećavao se s povećanjem tjelesne težine na nelinearan način. L "Poluvrijeme eliminacije plazme penciklovira se smanjivao sa smanjenjem dobi, sa prosječno 1,6 sati u bolesnika u dobi od 6 do 12 godina, na prosječno 1,2 sata u bolesnika u dobi od 6 do 12 godina. 1 do 2 godine nije dovršeno.
Starije osobe (≥ 65 godina)
Na temelju usporednih studija, nakon oralne primjene famciklovira prosječna vrijednost AUC bila je približno 30% veća, a bubrežni klirens penciklovira za približno 20% manji kod starijih dobrovoljaca (65-79 godina) u usporedbi s mlađim dobrovoljcima. Djelomično te razlike mogu biti posljedica razlika u bubrežnoj funkciji u dvije skupine. Nije potrebna prilagodba doze ovisno o dobi, pod uvjetom da bubrežna funkcija nije oštećena (vidjeti dio 4.2).
Seks
Zabilježene su male razlike u bubrežnom klirensu penciklovira između žena i muškaraca koje se pripisuju spolnim razlikama u bubrežnoj funkciji. Ovisno o spolu, nije potrebna prilagodba doze.
05.3 Pretklinički podaci o sigurnosti
Opća toksičnost
Studije farmakološke sigurnosti i toksičnosti pri ponovljenim dozama ne otkrivaju nikakve posebne rizike za ljude.
Genotoksičnost
Famciklovir nije bio genotoksičan u opsežnom nizu in vitro i in vivo testova koji su mogli otkriti mutaciju gena, kromosomska oštećenja i oštećenja DNK koja se mogu popraviti. Penciklovir je, slično drugim tvarima iste klase, uzrokovao kromosomska oštećenja, ali nije inducirao niti mutaciju gena u staničnim sustavima bakterija ili sisavaca, niti povećanje popravka DNA. in vitro.
Karcinogeneza
Povećana incidencija adenokarcinoma dojke, tumora koji se obično opaža kod ove vrste štakora, a koristi se u studijama karcinogenosti, zabilježena je pri visokim dozama kod ženki štakora. Nije bilo utjecaja na učestalost neoplazme kod mužjaka štakora ili miševa oba spola.
Reproduktivna toksičnost
Poremećena plodnost (uključujući patofiziološke promjene testisa, promijenjena morfologija spermija, smanjena koncentracija i pokretljivost spermija te smanjena plodnost) pronađena je kod mužjaka štakora koji su dobivali 500 mg / kg / dan. Osim toga, u studijama opće toksičnosti uočene su degenerativne promjene epitela testisa, koji je bio reverzibilan, a primijećen je i kod drugih tvari ove klase.Studije na životinjama nisu pokazale nikakve štetne učinke na plodnost žena.
06.0 FARMACEUTSKI PODACI
06.1 Pomoćne tvari
Famvir 125 i 250 mg filmom obložene tablete:
hidroksipropilceluloza, bezvodna laktoza, natrijev karboksimetil škrob, magnezijev stearat, hipromeloza, titanov dioksid (E 171), makrogol 4000, makrogol 6000.
Famvir 500 mg filmom obložene tablete:
hidroksipropil celuloza, natrijev karboksimetil škrob, magnezijev stearat, hipromeloza, titanov dioksid (E 171), makrogol 4000, makrogol 6000.
06.2 Nekompatibilnost
Nije bitno.
06.3 Razdoblje valjanosti
3 godine
06.4 Posebne mjere pri skladištenju
Ne čuvati na temperaturi iznad 30 ° C.
Famvir 500 mg filmom obložene tablete: čuvati u originalnom pakiranju radi zaštite lijeka od vlage.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja
Famvir 125 mg filmom obložene tablete
Blister pakiranja od 10 tableta po 125 mg
Famvir 250 mg filmom obložene tablete
Mjehurići od 15 i 21 tableta od 250 mg
Famvir 500 mg filmom obložene tablete
Mjehurići od 14 i 21 tablete od 500 mg
Ne mogu se na tržište staviti sve veličine pakiranja.
06.6 Upute za uporabu i rukovanje
Neiskorišteni lijek i otpad dobiven iz ovog lijeka moraju se zbrinuti u skladu s lokalnim propisima.
07.0 Nositelj odobrenja za stavljanje u promet
Novartis Farma S.p.A.
Largo Umberto Boccioni, 1
I - 21040 Origgio VA
08.0 BROJ DOZVOLE ZA PROMET
Famvir 125 mg filmom obložene tablete
10 tableta A.I.C. n. 029172044
Famvir 250 mg filmom obložene tablete
15 tableta A.I.C. n. 029172032
21 tableta A.I.C. n. 029172018
Famvir 500 mg filmom obložene tablete
14 tableta A.I.C. n. 029172069
21 tableta A.I.C. n. 029172057
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA
Famvir 250 mg filmom obložene tablete - 21 tableta:
Prva autorizacija: 01.06.1995
Obnova: 08.07.2011
Famvir 125 mg filmom obložene tablete - 10 tableta
Famvir 250 mg filmom obložene tablete - 15 tableta
Famvir 500 mg filmom obložene tablete - 14 tableta
Famvir 500 mg filmom obložene tablete - 21 tableta
Prva autorizacija: 07.05.2002
Obnova: 08.07.2011
10.0 DATUM REVIZIJE TEKSTA
Odredba AIFA -e od 17. veljače 2012