Aktivni sastojci: Sevelamer (sevelamer karbonat)
Renvela 800 mg filmom obložene tablete
Ulošci za paket Renvela dostupni su za veličine pakiranja:- Renvela 800 mg filmom obložene tablete
- Renvela 1,6 g prah za oralnu suspenziju
- Renvela 2,4 g prah za oralnu suspenziju
Indikacije Zašto se Renvela koristi? Čemu služi?
Renvela sadrži djelatnu tvar sevelamer karbonat koja djeluje sprječavajući apsorpciju fosfata prisutnog u hrani u probavni sustav i na taj način smanjuje razinu fosfata u krvi.
Renvela se koristi za kontrolu hiperfosfatemije (visoke razine fosfata u krvi) kod:
- odrasli pacijenti na dijalizi (tehnika uklanjanja krvi). Lijek se može koristiti u pacijenata na hemodijalizi (pomoću aparata za filtriranje krvi) ili peritonealnoj dijalizi (u kojoj se tekućina upumpava u trbuh, a unutarnja membrana tijela filtrira krv);
- Pacijenti s kroničnom bubrežnom bolešću koji nisu na dijalizi i imaju razinu fosfata u krvi jednaku ili veću od 1,78 mmol / L.
Renvela se mora koristiti s drugim tretmanima, poput dodataka kalcija i vitamina D, kako bi se spriječio razvoj bolesti kostiju.
Povećane razine fosfata u krvi mogu uzrokovati stvaranje čvrstih naslaga u tijelu koje se nazivaju kalcifikacije. Te naslage mogu ukrutiti krvne žile i otežati krv u distribuciji po tijelu. Osim toga, povećanje fosfata u krvi može uzrokovati svrbež kože, crvene oči, bolovi u kostima i prijelomi.
Kontraindikacije Kada se Renvela ne smije koristiti
Nemojte uzimati Renvela
- ako imate nisku razinu fosfata u krvi (liječnik će vas pregledati)
- ako patite od crijevne opstrukcije
- ako ste alergični na djelatnu tvar ili bilo koji drugi sastojak ovog lijeka (naveden u odjeljku 6).
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Renvela
Prije uzimanja lijeka Renvela razgovarajte sa svojim liječnikom ako se bilo što od sljedećeg odnosi na vas:
- problemi s gutanjem
- problemi s pokretljivošću (kretanjem) u želucu i crijevima
- učestalo povraćanje
- aktivna upala crijeva
- je podvrgnut velikoj operaciji želuca ili crijeva
Djeca i adolescenti
Sigurnost i djelotvornost u djece (mlađe od 18 godina) nisu ispitivane, pa se uporaba lijeka Renvela ne preporučuje u djece.
Daljnji tretmani:
Zbog bolesti bubrega ili liječenja dijalizom, možete:
- doživite nisku ili visoku razinu kalcija u krvi. Budući da Renvela ne sadrži kalcij, liječnik vam može propisati dodatke kalcija.
- imaju nisku razinu vitamina D u krvi. Zbog toga će vaš liječnik možda provjeriti razinu vitamina D u krvi i prema potrebi propisati dodatni vitamin D. Ako ne uzimate multivitaminske suplemente, možda ćete također imati niske razine vitamina A, E, K i folne kiseline u krvi, pa će vaš liječnik možda provjeriti te razine i prema potrebi propisati dodatke vitaminima.
Posebna napomena za pacijente na peritonealnoj dijalizi:
Možda imate peritonitis (infekcija abdominalne tekućine) povezan s peritonealnom dijalizom. Taj se rizik može smanjiti usvajanjem rigoroznih aseptičnih tehnika prilikom zamjene vrećica. Odmah obavijestite svog liječnika ako osjetite neke nove znakove ili simptome bolova u trbuhu, oticanje trbuha, bol u trbuhu, osjetljivost trbuha ili ukočenost trbuha, zatvor, vrućicu, zimicu, mučninu ili povraćanje.
Bit ćete podvrgnuti pažljivijim provjerama u slučaju problema povezanih s niskom razinom vitamina A, D, E, K i folne kiseline.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak lijeka Renvela
Obavijestite svog liječnika ako uzimate ili ste nedavno uzimali ili biste mogli uzeti bilo koje druge lijekove.
- Renvela se ne smije uzimati istodobno s ciprofloksacinom (antibiotikom).
- Ako uzimate lijekove za probleme srčanog ritma ili epilepsiju, posavjetujte se sa svojim liječnikom kada uzimate Renvela.
- Renvela može smanjiti učinke lijekova kao što su ciklosporin, mikofenolat mofetil i takrolimus (lijekovi koji se koriste za smanjenje aktivnosti imunološkog sustava). Vaš liječnik će vas savjetovati što učiniti ako uzimate ove lijekove.
- Istodobna primjena levotiroksina (lijeka za liječenje niske razine hormona štitnjače) i lijeka Renvela rijetko je rezultirala nedostatkom hormona štitnjače u nekih pacijenata. Zbog toga liječnik može pomnije pratiti razinu stimulirajućih hormona u krvi.
- Ako uzimate lijekove kao što su omeprazol, pantoprazol ili lansoprazol za liječenje žgaravice, gastroezofagealne refluksne bolesti ili čira na želucu, posavjetujte se sa svojim liječnikom kada uzimate Renvela.
Vaš liječnik će redovito provjeravati ima li interakcija između lijeka Renvela i drugih lijekova.
U nekim slučajevima, kada se Renvela mora uzimati istodobno s drugim lijekom, liječnik vam može savjetovati da uzmete ovaj lijek 1 sat prije ili 3 sata nakon uzimanja Renvela ili razmislite o provjeri razine tog lijeka u krvi.
Upozorenja Važno je znati da:
Trudnoća i dojenje
Ako ste trudni ili dojite, mislite da ste trudni ili planirate trudnoću, pitajte svog liječnika za savjet prije nego uzmete ovaj lijek. Nije poznato utječe li Renvela na fetus.
Recite svom liječniku ako želite dojiti svoju bebu. Nije poznato može li Renvela proći kroz majčino mlijeko i utjecati na bebu.
Upravljanje vozilima i strojevima
Nije vjerojatno da će Renvela utjecati na sposobnost upravljanja vozilima i rada sa strojevima.
Doza, način i vrijeme primjene Kako se koristi Renvela: Doziranje
Renvela morate uzeti točno onako kako vam je rekao liječnik. Vaš će liječnik dozu temeljiti na razini fosfata u krvi.
Preporučena početna doza Renvela tableta za odrasle i starije osobe (starije od 65 godina) je jedna ili dvije tablete od 800 mg, 3 puta dnevno uz glavne obroke.
Tablete treba progutati cijele. Nemojte drobiti, žvakati ili lomiti tablete.
Vaš će liječnik u početku provjeravati razinu fosfata u krvi svaka 2-4 tjedna i po potrebi može prilagoditi dozu lijeka Renvela kako bi dosegao odgovarajuću razinu fosfata.
Pacijenti koji uzimaju Renvela moraju se pridržavati propisane prehrane.
Ako ste zaboravili uzeti Renvelu
Ako ste propustili uzeti dozu, sljedeću dozu uzmite u uobičajeno vrijeme uz obrok. Nemojte uzeti dvostruku dozu kako biste nadoknadili zaboravljenu.
Predoziranje Što učiniti ako ste uzeli previše lijeka Renvela
U slučaju mogućeg predoziranja, odmah se obratite svom liječniku.
Nuspojave Koje su nuspojave lijeka Renvela
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih.
Budući da zatvor može biti rani simptom začepljenja crijeva, obavijestite svog liječnika ili ljekarnika.
Sljedeće nuspojave zabilježene su u pacijenata koji su uzimali Renvela:
Vrlo često (mogu se javiti u više od 1 na 10 korisnika):
Povraćanje, zatvor, bol u gornjem dijelu trbuha, mučnina.
Česte (mogu se javiti u do 1 na 10 korisnika):
Proljev, bolovi u trbuhu, probavne smetnje, nadutost.
Vrlo rijetko (mogu se javiti u do 1 korisnika na 10.000):
Preosjetljivost.
Nije poznato (učestalost se ne može procijeniti iz dostupnih podataka):
Bilo je izvješća o svrbežu, osipu, usporenoj pokretljivosti crijeva (kretanju) / začepljenju crijeva i perforaciji crijevne stjenke.
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku koji uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Također možete prijaviti nuspojave izravno putem nacionalnog sustava prijavljivanja navedenih u Dodatku V. Prijavljivanjem nuspojava možete pomoći u pružanju više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
Čuvajte ovaj lijek izvan pogleda i dohvata djece.
Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na bočici i kutiji iza "EXP".
Spremnik držati dobro zatvoren radi zaštite od vlage.
Ovaj lijek ne zahtijeva nikakve posebne uvjete skladištenja.
Nemojte bacati lijekove u otpadne vode ili kućni otpad. Pitajte ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Rok "> Ostale informacije
Što Renvela sadrži
- Aktivni sastojak je sevelamer karbonat. Svaka filmom obložena tableta Renvela sadrži 800 mg sevelamer karbonata.
- Pomoćni sastojci su mikrokristalna celuloza, natrijev klorid i cinkov stearat. Obloga tablete sadrži hipromelozu (E464) i diacetilirane monogliceride. Tiskarska boja sadrži crni željezov oksid (E172), izopropil alkohol, propilen glikol i hipromelozu (E464).
Kako Renvela izgleda i sadržaj pakiranja
Renvela filmom obložene tablete su bijele tablete s ugraviranim RENVELA 800 na jednoj strani.
Tablete su pakirane u polietilenske boce velike gustoće, opremljene polipropilenskim poklopcem i indukcijskim zatvaračem.
Ambalaža:
- 1 x 30 tableta po bočici
- 1 x 180 tableta po bočici
- 180 tableta (6 bočica po 30 tableta)
Ne mogu se na tržište staviti sve veličine pakiranja.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA -
RENVELA 800 MG TABLETE OBLOŽENE FILMOM
02.0 KVALITATIVNI I KOLIČINSKI SASTAV -
Svaka tableta sadrži 800 mg sevelamer karbonata.
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK -
Filmom obložena tableta (tableta).
Bijele do gotovo bijele tablete s jedne strane imaju oznaku "RENVELA 800".
04.0 KLINIČKI PODACI -
04.1 Terapeutske indikacije -
Renvela je indicirana za kontrolu hiperfosfatemije kod odraslih pacijenata na hemodijalizi ili peritonealnoj dijalizi.
Renvela je također indicirana u kontroli hiperfosfatemije kod odraslih pacijenata s kroničnom bubrežnom bolešću koji nisu na dijalizi sa serumskim fosforom> 1,78 mmol / l.
Renvela bi se trebala koristiti u kontekstu multi-terapeutskog pristupa koji bi mogao uključivati dodatke kalcija, 1,25-dihidroksi-vitamin D3 ili jedan od njegovih analoga za kontrolu razvoja bubrežne koštane bolesti.
04.2 Doziranje i način primjene -
Doziranje
Početna doza
Preporučena početna doza za sevelamer karbonat je 2,4 g ili 4,8 g dnevno, na temelju kliničkih potreba i razine fosfora u serumu. Renvela se mora uzimati tri puta dnevno, uz obrok.
* Plus naknadna titracija prema uputama
Kod pacijenata koji su prethodno uzimali vezivo za fosfate (sevelamer hidroklorid ili na bazi kalcija), Renvela se mora primjenjivati na osnovi gram po gram, uz praćenje razine fosfata kako bi se osigurale optimalne dnevne doze.
Titracija i održavanje
Treba pratiti razinu fosfata i titrirati dozu sevelamer karbonata u koracima od 0,8 g tri puta dnevno (2,4 g / dan) svaka 2-4 tjedna dok se ne postigne prihvatljiva razina fosfora u serumu, nakon čega slijedi redovito praćenje.
Pacijenti koji uzimaju Renvela moraju se pridržavati propisane dijete.
U kliničkoj praksi liječenje će biti kontinuirano, na temelju potrebe kontrole razine fosfata, očekivana doza bit će u prosjeku oko 6 g dnevno.
Pedijatrijska populacija
Sigurnost i djelotvornost lijeka Renvela nisu utvrđene u djece mlađe od 18 godina.
Način primjene
Oralna upotreba.
Tablete se trebaju progutati cijele i ne smiju se drobiti, žvakati ili drobiti prije primjene
04.3 Kontraindikacije -
• Preosjetljivost na djelatnu tvar ili neku od pomoćnih tvari navedenih u dijelu 6.1.
• Hipofosfatemija
• Opstrukcija crijeva.
04.4 Posebna upozorenja i mjere opreza pri uporabi -
Sigurnost i djelotvornost lijeka Renvela nisu utvrđene kod odraslih pacijenata s kroničnom bubrežnom bolešću koji nisu na dijalizi sa serumskim fosforom.
Sigurnost i djelotvornost lijeka Renvela nisu utvrđene u pacijenata sa sljedećim poremećajima:
• disfagija
• smetnje gutanja
• teški poremećaji gastrointestinalne pokretljivosti, uključujući tešku ili neliječenu gastroparezu, zadržavanje želučanog sadržaja i abnormalnu ili nepravilnu pokretljivost crijeva
• aktivna upalna bolest crijeva
• velike operacije na gastrointestinalnom traktu
Stoga je potreban oprez u primjeni lijeka Renvela u ovih bolesnika.
Crijevna opstrukcija i ileus / subileus
U vrlo rijetkim slučajevima opažena je opstrukcija crijeva i ileus / subileus u bolesnika tijekom liječenja sevelamerijevim kloridom (kapsule / tablete), koji sadrži istu aktivnu skupinu kao i sevelamer karbonat. Zatvor može biti prodrom. Pacijente koji pate od zatvora potrebno je pomno pratiti tijekom liječenja lijekom Renvela. Liječenje lijekom Renvela treba ponovno procijeniti u pacijenata koji razviju teški zatvor ili druge teške gastrointestinalne simptome.
Vitamini topljivi u mastima
Pacijenti sa kroničnom bubrežnom bolešću (kronična bolest bubrega, kronična bolest bubrega) može pokazati nedostatak vitamina A, D, E i K topljivih u mastima, ovisno o prehrani i težini bolesti. Nije isključeno da se Renvela može vezati za vitamine topive u mastima sadržane u unesenoj hrani. U bolesnika koji uzimaju sevelamer, ali bez vitaminskih dodataka, treba redovito procjenjivati serumske razine vitamina A, D, E i K. Po potrebi se preporučuju vitaminski dodaci. Dodaci vitamina D (približno 400 IU prirodnog vitamina D dnevno) preporučuju se bolesnicima s kroničnom bubrežnom insuficijencijom koji nisu na dijalizi, što može biti dio multivitaminskog pripravka koji se uzima iz doze Renvela. U bolesnika na peritonealnoj dijalizi preporučuje se dodatno praćenje vitamina topljivih u mastima i folne kiseline, budući da razine vitamina A, D, E i K nisu mjerene u kliničkom ispitivanju ovih pacijenata.
Nedostatak folata
Trenutno nema dovoljno podataka da bi se isključila mogućnost nedostatka folne kiseline tijekom dugotrajnog liječenja lijekom Renvela.
Hipokalcemija / hiperkalcemija
Bolesnici s kroničnom bubrežnom bolešću mogu razviti hipokalcemiju ili hiperkalcemiju. Renvela ne sadrži kalcij. Zbog toga je potrebno redovito pratiti razinu kalcija u serumu i prema potrebi primjenjivati dodatak elementarnog kalcija.
Metabolička acidoza
Pacijenti s kroničnom bubrežnom bolešću skloni su "metaboličkoj acidozi. U sklopu dobre kliničke prakse stoga se preporučuje praćenje razine bikarbonata u serumu".
Peritonitis
Pacijenti na dijalizi podložni su određenom riziku od infekcije svojstvenom specifičnom načinu dijalize. Peritonitis je poznata komplikacija u bolesnika na peritonealnoj dijalizi, a zabilježeno je više slučajeva peritonitisa u skupini koja je primala sevelamer nego u kontrolnoj skupini u kliničkoj studiji sevelamer hidroklorida. Pacijente koji primaju peritonealnu dijalizu treba pomno pratiti kako bi se osiguralo korištenje ispravne aseptičke tehnike te pravodobna identifikacija i liječenje svih znakova i simptoma povezanih s peritonitisom.
Poteškoće pri gutanju i gušenju
Rijetko su prijavljene poteškoće pri gutanju tableta Renvela. Mnogi od ovih slučajeva uključivali su pacijente s komorbidnim stanjima, uključujući poremećaje gutanja ili abnormalnosti jednjaka. Stoga je potreban oprez kada se Renvela primjenjuje kod pacijenata s poteškoćama u gutanju. Renvela prašak za oralnu suspenziju treba koristiti za pacijente s poviješću poteškoća s gutanjem.
Hipotireoza
Preporuča se pomnije praćenje bolesnika s hipotireozom istodobno primijenjenih sa sevelamer karbonatom i levotiroksinom (vidjeti dio 4.5).
Dugotrajno kronično liječenje
U jednogodišnjoj kliničkoj studiji nije bilo dokaza o nakupljanju sevelamera. Međutim, mogućnost apsorpcije i akumulacije sevelamera u kroničnom dugotrajnom (> godinu dana) liječenju ne može se u potpunosti isključiti (vidjeti dio 5.2).
Hiperparatireoidizam
Renvela nije indicirana za kontrolu hiperparatireoidizma. U pacijenata sa sekundarnim hiperparatireoidizmom, Renvela se mora koristiti u kontekstu multi-terapijskog pristupa, koji može uključivati nadomjestke kalcija, 1,25-dihidroksi-vitamin D3 ili jedan od njegovih analoga, kako bi se smanjila netaknute razine paratiroidnih hormona (iPTH).
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija -
Dijaliza
Nisu provedena ispitivanja interakcija kod pacijenata na dijalizi.
Ciprofloksacin
U studijama interakcije na zdravim dobrovoljcima, sevelamer hidroklorid, koji sadrži istu aktivnu skupinu kao i Renvela, smanjio je bioraspoloživost ciprofloksacina za približno 50% uz istovremenu primjenu sevelamer hidroklorida u studiji s jednom dozom. Stoga se Renvela ne smije uzimati u u isto vrijeme kao i ciprofloksacin.
Ciklosporin, mofetil mikofenolat i takrolimus u transplantiranih pacijenata
Smanjene razine ciklosporina, mofetilmikofenolata i takrolimusa zabilježene su kod primatelja transplantata, uz istodobnu primjenu sa sevelamer hidrokloridom, bez kliničkih posljedica (npr. Odbijanje transplantata). Interakcije se ne mogu isključiti, stoga je potrebno razmotriti pažljivo praćenje koncentracija ciklosporina, mofetilmikofenolata i takrolimusa u krvi tijekom primjene kombinacije i nakon prestanka primjene.
Levotiroksin
Vrlo rijetki slučajevi hipotireoze zabilježeni su u bolesnika koji su istodobno uzimali sevelamer hidroklorid, koji sadrži istu aktivnu skupinu kao i sevelamer karbonat, i levotiroksin. Stoga se preporučuje pažljivo praćenje razine stimulirajućeg hormona štitnjače (TSH) u bolesnika koji primaju sevelamer karbonat i levotiroksin.
Antiarimični i antikonvulzivni lijekovi
Pacijenti koji su uzimali antiaritmike za kontrolu aritmija i antikonvulzive za kontrolu poremećaja napada bili su isključeni iz kliničkih ispitivanja. Potreban je oprez pri propisivanju lijeka Renvela pacijentima koji također uzimaju ove lijekove.
Digoksin, varfarin, enalapril ili metoprolol
U studijama interakcija na zdravim dobrovoljcima, sevelamer hidroklorid, koji sadrži isti aktivni dio kao i sevelamer karbonat, nije imao utjecaja na bioraspoloživost digoksina, varfarina, enalaprila ili metoprolola.
Bioraspoloživost
Renvela se ne apsorbira i može utjecati na bioraspoloživost drugih lijekova. Prilikom primjene bilo kojeg lijeka, gdje bi bilo kakvo smanjenje bioraspoloživosti imalo klinički značajan učinak na sigurnost ili djelotvornost, lijek treba primijeniti najmanje jedan sat prije ili najmanje tri sata nakon uzimanja lijeka Renvela. Alternativno, liječnik bi trebao razmotriti provjeru razine u krvi.
04.6 Trudnoća i dojenje -
Trudnoća
Nema ili su ograničeni podaci o uporabi sevelamera u trudnica. Studije na životinjama pokazale su reproduktivnu toksičnost pri primjeni sevelamera u visokim dozama kod štakora (vidjeti dio 5.3). Također je dokazano da sevelamer smanjuje apsorpciju nekoliko vitamine, uključujući folnu kiselinu (vidjeti dijelove 4.4 i 5.3). Potencijalni rizik za ljude je nepoznat. Renvela se smije primjenjivati trudnicama samo ako je to jasno potrebno i nakon „pažljive analize omjera rizika i koristi za majku i za fetus.
Vrijeme za hranjenje
Nije poznato izlučuju li se sevelamer / metaboliti u majčino mlijeko u ljudi. Činjenica da se sevelamer ne apsorbira čini njegovo izlučivanje u majčino mlijeko malo vjerojatnim. Odluka o nastavku / prekidu dojenja ili nastavku / prekidu terapije lijekom Renvela mora se donijeti uzimajući u obzir dobrobit dojenja za dijete i korist terapije lijekom Renvela za ženu.
Plodnost
Nema podataka o učinku sevelamera na plodnost ljudi. Studije na životinjama pokazale su da sevelamer nije utjecao na plodnost kod mužjaka i ženki štakora pri izloženosti ekvivalentnoj dozi kod ljudi dvostruko većoj od maksimalne doze u kliničkom ispitivanju od 13 g / dan na temelju usporedbe relativne tjelesne površine.
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima -
Sevelamer nema ili ima zanemariv utjecaj na sposobnost upravljanja vozilima i rada sa strojevima.
04.8 Nuspojave -
Sažetak sigurnosnog profila
Najčešće nuspojave (> 5% bolesnika) spadale su u gastrointestinalne poremećaje prema organskim sustavima. Većina ovih nuspojava bila je blagog do umjerenog intenziteta.
Tablica nuspojava
Sigurnost sevelamera (i u obliku karbonatnih soli i u hidrokloridu) ispitivana je u brojnim kliničkim studijama koje su uključivale ukupno 969 pacijenata na hemodijalizi, a tretmani su trajali 4 - 50 tjedana (724 bolesnika liječenih sevelamer hidrokloridom i 245 s sevelamer karbonatom), 97 bolesnici na peritonealnoj dijalizi s 12-tjednim liječenjem (svi su liječeni sevelamerijevim kloridom) i 128 nedijaliziranih bolesnika sa kroničnom bubrežnom insuficijencijom na liječenju 8-12 tjedana (liječenje 79 pacijenata sa sevelamer hidrokloridom i 49 s sevelamer karbonatom).
Nuspojave su prema učestalosti navedene u donjoj tablici. Učestalost prijavljivanja klasificirana je kao vrlo česta (> 1/10), česta (> 1/100, 1/1000, 1/10000,
Prijavljivanje sumnji na nuspojave
Izvještavanje o sumnji na nuspojave koje se jave nakon odobrenja lijeka važno je jer omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih djelatnika se traži da prijavljuju sve sumnje na nuspojave putem nacionalnog sustava prijavljivanja. U "Prilogu V. .
04.9 Predoziranje -
Sevelamer hidroklorid, koji sadrži istu aktivnu frakciju kao i sevelamer karbonat, davan je normalnim zdravim dobrovoljcima u dozama do 14 grama dnevno tijekom osam dana, bez izazivanja neželjenih učinaka. U bolesnika s kroničnom bubrežnom bolešću, najveća dnevna doza koja je proučavana bila je u prosjeku 14,4 grama sevelamer karbonata u jednoj dnevnoj dozi.
05.0 FARMAKOLOŠKA SVOJSTVA -
05.1 "Farmakodinamička svojstva -
Farmakoterapijska skupina: liječenje hiperfosfatemije.
ATC oznaka: V03A E02.
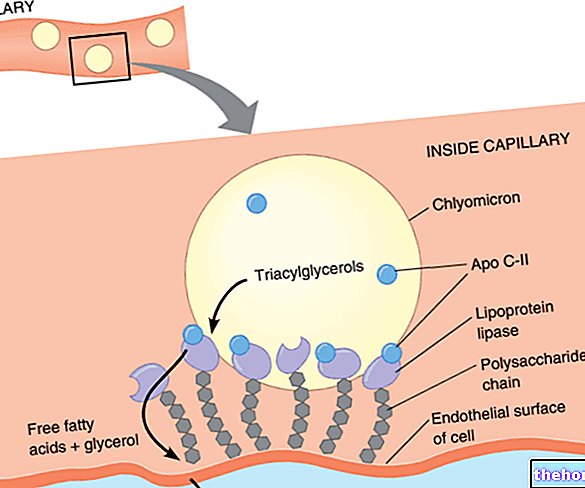
Renvela sadrži sevelamer, umreženi polimer koji se ne apsorbira, fosfatira i ne sadrži metale ili kalcij. Sevelamer sadrži više amina odvojenih ugljikom od jezgre strukture polimera, koji postaje protoniran u želucu. Ti protonirani amini negativno vežu nabijene ione, poput fosfata u prehrani, u crijevima. Vezivanjem fosfata u crijevnom traktu i slabljenjem njegove apsorpcije, sevelamer smanjuje serumsku koncentraciju fosfora.Riječno praćenje razine fosfata neizostavno je potrebno tijekom primjene veziva fosfata.
U dva randomizirana, unakrsna klinička ispitivanja, pokazalo se da je sevelamer karbonat, u obliku tableta i u prahu, terapijski ekvivalentan sevelamerijevom kloridu kada se primjenjuje tri puta dnevno, te je stoga učinkovit u kontroli fosfatemije u bolesnika s KBK -om na hemodijalizi.
Prva studija pokazala je da je uzimanje sevelamer karbonata tri puta dnevno ekvivalentno tabletama sevelamer hidroklorida tri puta dnevno u 79 pacijenata na hemodijalizi liječenih tijekom dva 8-tjedna randomizirana razdoblja terapije (s prosječnim ponderiranim prosječnim serumskim fosfatom od 1,5 ± 0,3 mmol / l i za sevelamer karbonat i za sevelamer hidroklorid). Druga studija pokazala je ekvivalenciju između praha sevelamer karbonata, primijenjenog tri puta dnevno, i tableta sevelamer hidroklorida koje se daju tri puta dnevno 31 bolesniku na hemodijalizi s hiperfosfatemijom (definiranom kao razina fosfata u serumu> 1,78 mmol / l), u rasponu od dva 4- tjedni randomizirani periodi liječenja (s prosječnim vremenski ponderiranim prosječnim serumskim fosfatom od 1,6 ± 0,5 mmol / l za prah sevelamer karbonata i 1,7 ± 0,4 mmol / l za tablete sevelamer hidroklorida).
U kliničkim ispitivanjima na bolesnicima na hemodijalizi, sam sevelamer nije pokazao dosljedan i klinički značajan učinak na razinu intaktnog paratiroidnog hormona (iPTH) u serumu. U 12-tjednom ispitivanju pacijenata na peritonealnoj dijalizi primijećeno je smanjenje iPTH-a slično onima kod pacijenata koji su primali kalcijev acetat. U bolesnika sa sekundarnim hiperparatireoidizmom, Renvela se mora koristiti u kontekstu višestrukog terapijskog pristupa, koji bi mogao uključivati kalcij kao suplemente, 1,25-dihidroksi-vitamin D3 ili jedan od njegovih analoga, za smanjenje intaktnog paratiroidnog hormona (iPTH).
Dokazano je vezanje sevelamera na žučne kiseline in vitro I in vivo, u eksperimentalnim životinjskim modelima. Vezanje žučne kiseline smolama za izmjenu iona dokazana je metoda za snižavanje kolesterola u krvi. U kliničkim studijama na sevelameru, i ukupni kolesterol i LDL kolesterol pali su za 15-39%. Smanjenje kolesterola opaženo je nakon 2. tjedana liječenja i održava se dugotrajnim liječenjem .. Trigliceridi, HDL kolesterol i albumin nisu se promijenili nakon liječenja sevelamerom.
Budući da sevelamer veže žučne kiseline, može ometati apsorpciju vitamina topljivih u mastima, poput vitamina A, D, E i K.
Sevelamer ne sadrži kalcij i smanjuje učestalost hiperkalcemijskih epizoda, u usporedbi sa pacijentima koji uzimaju samo vezivna sredstva na bazi kalcija. Pokazalo se da se učinci sevelamera na fosfor i kalcij održavaju tijekom čitavog praćenja. -Up od jedne godine Ove su informacije dobivene iz studija u kojima je korišten sevelamer hidroklorid.
05.2 "Farmakokinetička svojstva -
Farmakokinetička ispitivanja sevelamer karbonata nisu provedena. Sevelamer hidroklorid, koji sadrži isti aktivni dio kao i sevelamer karbonat, ne apsorbira se iz gastrointestinalnog trakta, što je potvrđeno studijom apsorpcije na zdravim dobrovoljcima.
05.3 Pretklinički sigurnosni podaci -
Neklinički podaci o sevelameru ne otkrivaju posebnu opasnost za ljude na temelju konvencionalnih studija farmakološke sigurnosti, toksičnosti pri ponovljenim dozama ili genotoksičnosti.
Studije karcinogenosti s oralnim sevelamer hidrokloridom provedene su na miševima (doze do 9 g / kg / dan) i štakorima (0,3, 1 ili 3 g / kg / dan). Postojala je "povećana incidencija prolaznih staničnih papiloma mokraćnog mjehura u muških štakora, u skupini s visokim dozama (ekvivalentna doza za čovjeka dvostruko veća od maksimalne doze od 14,4 g u kliničkom ispitivanju). Nije bilo povećanja incidence. Tumori u miševa ( ekvivalentna doza čovjeka trostruko povećala maksimalnu dozu u kliničkim ispitivanjima).
U citogenetskom testu in vitro u sisavaca, uz metaboličku aktivaciju, sevelamer hidroklorid uzrokovao je statistički značajno povećanje broja strukturnih kromosomskih aberacija. Sevelamer hidroklorid nije bio mutagen u testu Ames bakterijske mutacije.
Kod štakora i pasa sevelamer je smanjio apsorpciju vitamina D, E i K topljivih u mastima (faktori zgrušavanja) i folne kiseline.
Nedostaci okoštavanja kostura uočeni su na različitim mjestima u fetusa ženki štakora koji su primali sevelamer u srednjim i visokim dozama (ekvivalentna doza kod ljudi ispod maksimalne doze od 14,4 g). Ovi učinci mogu biti sekundarni zbog iscrpljivanja vitamina D.
U trudnih kunića koji su oralno primali sevelamerijev klorid uz pomoć sonde, došlo je do povećanja rane resorpcije u skupini s visokim dozama tijekom organogeneze (ekvivalentna doza čovjeka dvostruko veća od maksimalne doze u skupini s visokim dozama). Klinička ispitivanja).
Sevelamer hidroklorid nije ugrozio plodnost mužjaka ili ženke štakora u studiji o primjeni hrane u kojoj su ženke liječene 14 dana prije parenja do gestacije, a mužjaci 28 dana prije gestacije. Maksimalna doza u ovoj studiji bila je 4,5 g / kg / dan (ekvivalentna doza za čovjeka dvostruko veća od maksimalne doze u kliničkim studijama od 13 g / dan, na temelju usporedbe relativne tjelesne površine).
06.0 FARMACEUTSKE INFORMACIJE -
06.1 Pomoćne tvari -
Tableta:
Mikrokristalna celuloza
Natrijev klorid
Cinkov stearat
Premazni film:
Hipromeloza (E464)
Diacetilirani monogliceridi
Tiskarska tinta:
Crni željezov oksid (E172)
Propilen glikol
Izopropil alkohol
Hipromeloza (E464)
06.2 Inkompatibilnost "-
Nije bitno.
06.3 Rok valjanosti "-
3 godine.
06.4 Posebne mjere pri skladištenju -
Bočicu dobro zatvorite kako biste zaštitili lijek od vlage.
Ovaj lijek ne zahtijeva posebne temperature skladištenja.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja -
HDPE boce opremljene polipropilenskim čepom i aluminijskim indukcijskim zatvaračem.
Svaka bočica sadrži 30 tableta ili 180 tableta.
Pakiranja od 30 ili 180 tableta i višestruko pakiranje koje sadrži 180 (6 bočica s 30) tableta.
Ne mogu se na tržište staviti sve veličine pakiranja.
06.6 Upute za uporabu i rukovanje -
Neiskorišteni lijek i otpad dobiven iz ovog lijeka moraju se zbrinuti u skladu s lokalnim propisima.
07.0 NOSITELJ "Odobrenja za stavljanje u promet" -
Genzyme Europe B.V.
Gooimeer 10
1411 DD Naarden
Nizozemska
08.0 BROJ DOZVOLE ZA PROMET -
EU/1/09/521/001
039480013
EU/1/09/521/002
039480025
EU/1/09/521/003
039480037
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA -
Datum prve autorizacije: 10. lipnja 2009
10.0 DATUM REVIZIJE TEKSTA -
Ožujka 2014