Aktivni sastojci: Rupatadin
Rupafin tablete od 10 mg
Indikacije Zašto se koristi Rupafin? Čemu služi?
Rupatadin je antihistaminik.
Rupafin ublažava simptome alergijskog rinitisa poput kihanja, curenja iz nosa, svrbeža u očima i nosu.
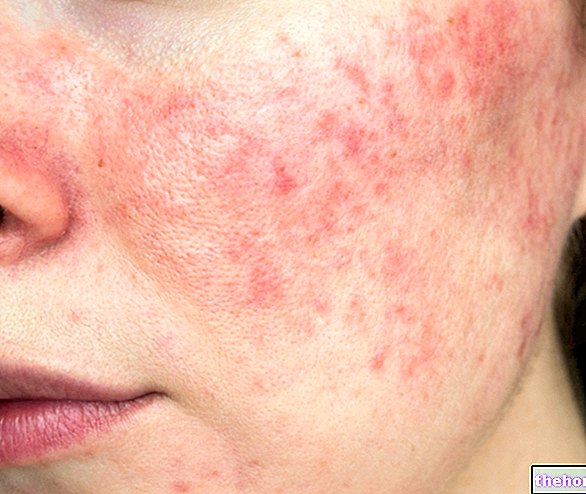
Rupafin se također koristi za ublažavanje simptoma povezanih s kroničnom idiopatskom urtikarijom (alergijski osip na koži), poput svrbeža i žuljeva (lokalizirano crvenilo i oticanje kože).
Kontraindikacije Kada se Rupafin ne smije koristiti
Nemojte uzimati Rupafin
- ako ste alergični na rupatadin ili neki drugi sastojak ovog lijeka
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Rupafin
Prije nego počnete uzimati Rupafin, razgovarajte sa svojim liječnikom ili ljekarnikom.
U slučaju zatajenja bubrega ili jetre, obratite se svom liječniku. Trenutačno se ne preporučuje uporaba rupafina u tabletama od 10 mg u bolesnika s oštećenjem bubrega ili jetre.
Ako imate niske razine kalija u krvi i / ili imate nenormalan obrazac otkucaja srca (poznato produljenje QTc intervala na EKG -u) koji se može pojaviti u nekim oblicima srčanih bolesti, pitajte svog liječnika za savjet.
Ako ste stariji od 65 godina, posavjetujte se sa svojim liječnikom ili ljekarnikom.
Djeca
Ovaj lijek nije indiciran za djecu mlađu od 12 godina.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak rupafina
Obavijestite svog liječnika ili ljekarnika ako uzimate, nedavno ste uzimali ili biste mogli uzeti bilo koje druge lijekove.
Nemojte uzimati lijekove koji sadrže ketokonazol ili eritromicin ako koristite Rupafin.
Ako uzimate lijekove protiv depresije središnjeg živčanog sustava ili statine, razgovarajte sa svojim liječnikom prije nego uzmete Rupafin.
Rupafin s hranom, pićem i alkoholom
Rupafin se ne smije uzimati sa sokom od grejpa, jer ovaj napitak može povećati razinu rupafina u tijelu.
Rupafin, u preporučenoj dozi (10 mg), ne povećava pospanost koju stvara alkohol.
Upozorenja Važno je znati da:
Trudnoća i dojenje
Ako ste trudni ili dojite, mislite da ste trudni ili planirate trudnoću, obratite se svom liječniku ili ljekarniku za savjet prije nego uzmete ovaj lijek.
Upravljanje vozilima i strojevima
U preporučenim dozama nema poznatih učinaka Rupafina na sposobnost upravljanja vozilima i rada sa strojevima. Međutim, pri započinjanju liječenja Rupafinom, morate biti oprezni i pratiti utjecaj liječenja na vas prije vožnje ili rada sa strojevima.
Rupafin sadrži laktozu.
Ako vam je liječnik rekao da ne podnosite neke šećere, obratite se svom liječniku prije uzimanja ovog lijeka.
Doza, način i vrijeme primjene Kako koristiti Rupafin: Doziranje
Uvijek uzimajte ovaj lijek točno onako kako vam je rekao liječnik. Ako ste u nedoumici, obratite se svom liječniku ili ljekarniku.
Rupafin je indiciran za adolescente (starije od 12 godina) i za odrasle. Uobičajena doza je jedna tableta (10 mg rupatadina) jednom dnevno na pun ili prazan želudac. Tabletu progutajte s dovoljnom količinom tekućine (npr. Čašom vode).
Trajanje liječenja Rupafinom naznačit će liječnik.
Predoziranje Što učiniti ako ste uzeli previše Rupafina
Ako ste uzeli više Rupafina nego što je trebalo
Odmah se obratite svom liječniku ili ljekarniku ako ste slučajno uzeli preveliku dozu lijeka.
Ako ste zaboravili uzeti Rupafin
Uzmite dozu što je prije moguće i nastavite s uobičajenom dozom. Nemojte uzeti dvostruku dozu kako biste nadoknadili zaboravljene pojedinačne doze
Nuspojave Koje su nuspojave Rupafina
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih.
Česte nuspojave (mogu se javiti u do 1 na 10 osoba) su pospanost, glavobolja, omaglica, suha usta, osjećaj slabosti i umora.
Manje česte nuspojave (mogu se pojaviti u do 1 na 100 osoba) su povećani apetit, razdražljivost, poremećaj pažnje, nazalno krvarenje, suhoća nosa, faringitis, kašalj, suhoća u grlu, rinitis, mučnina, bol u trbuhu, proljev, probavne smetnje, povraćanje, zatvor, osip, bolovi u leđima, bolovi u zglobovima, bolovi u mišićima, žeđ, opći osjećaj nelagode, vrućica, abnormalni testovi funkcije jetre i debljanje.
Rijetke nuspojave (mogu se javiti u do 1 na 1000 osoba) su lupanje srca, povećani broj otkucaja srca i alergijske reakcije (svrbež, žuljevi i oticanje lica, usana, jezika ili usta).
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku ili ljekarniku.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Također možete prijaviti nuspojave izravno putem nacionalnog sustava za prijavljivanje na https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse Prijavljivanjem nuspojava možete pomoći u pružanju više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
Čuvajte ovaj lijek izvan pogleda i dohvata djece.
Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na kutiji i blisteru. Datum isteka odnosi se na zadnji dan tog mjeseca.
Čuvajte blister u vanjskom pakiranju kako biste zaštitili lijek od svjetlosti.
Ne bacajte lijekove u otpadne vode ili kućni otpad. Pitajte ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Što Rupafin sadrži
- Aktivni sastojak je rupatadin. Svaka tableta sadrži 10 mg rupatadina (u obliku fumarata).
- Ostali sastojci su preželatinizirani kukuruzni škrob, mikrokristalna celuloza, crveni željezov oksid (E-172), žuti željezov oksid (E-172), laktoza monohidrat i magnezijev stearat.
Opis izgleda Rupafina i sadržaj pakiranja
Rupafin dolazi u obliku okruglih, svijetlih tableta boje lososa, pakiranih u blistere koji sadrže 3, 7, 10, 15, 20, 30, 50 i 100 tableta. Ne mogu se na tržište staviti sve veličine pakiranja.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA
RUPAFIN 10 MG TABLETE
02.0 KVALITATIVNI I KOLIČINSKI SASTAV
Svaka tableta sadrži:
10 mg rupatadina (u obliku fumarata).
Pomoćna tvar s poznatim učinkom: 58 mg laktoze u obliku laktoze monohidrata.
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK
Tableta.
Okrugle, svijetle tablete boje lososa.
04.0 KLINIČKI PODACI
04.1 Terapeutske indikacije
Simptomatsko liječenje alergijskog rinitisa i kronične idiopatske urtikarije u odraslih i adolescenata (starijih od 12 godina).
04.2 Doziranje i način primjene
Odrasli i adolescenti (stariji od 12 godina)
Preporučena doza je 10 mg (jedna tableta) jednom dnevno, sa ili bez hrane.
Umirovljenici
Rupatadin se mora koristiti s oprezom u starijih osoba (vidjeti dio 4.4).
Pedijatrijski bolesnici
Primjena 10 mg rupatadina u tabletama ne preporučuje se u djece mlađe od 12 godina.Rupatadin 1 mg / ml oralna otopina preporučuje se u djece od 2 do 11 godina.
Bolesnici s bubrežnom ili jetrenom insuficijencijom
Nema kliničkog iskustva u bolesnika s oštećenom bubrežnom ili jetrenom funkcijom, trenutno se ne preporučuje davanje ovih pacijenata 10 mg rupatadina.
04.3 Kontraindikacije
Preosjetljivost na djelatnu tvar ili neku od pomoćnih tvari navedenih u dijelu 6.1.
04.4 Posebna upozorenja i mjere opreza pri uporabi
Ne preporučuje se primjena rupatadina sa sokom od grejpa (vidjeti dio 4.5).
Istodobnu primjenu rupatadina s snažnim inhibitorima CYP3A4 treba izbjegavati, dok ga treba davati s oprezom s umjerenim inhibitorima CYP3A4 (vidjeti dio 4.5).
Može biti potrebno prilagođavanje doze osjetljivih supstrata CYP3A4 (npr. Simvastatin, lovastatin) i supstrata CYP3A4 s uskim terapijskim prozorom (npr. Ciklosporin, takrolimus, sirolimus, everolimus, cisaprid) jer rupatadin može povećati koncentraciju ovih lijekova u plazmi (vidjeti dio 4.5).
Srčana sigurnost rupatadina procijenjena je temeljitom studijom QT / QTc. Rupatadin do deset puta veći od terapijske doze nije imao učinka na EKG -u i stoga nije izazvao zabrinutost za srčanu sigurnost. Međutim, rupatadin se mora koristiti s oprezom u bolesnika s prepoznatim produljenjem QT intervala, u bolesnika s "nekorigiranom hipokalijemijom, u pacijenata s tekućim proaritmijskim stanjima, kao što je klinički značajna bradikardija, akutna ishemija miokarda.
Rupatadin 10 mg tablete treba koristiti s oprezom u starijih bolesnika (65 godina ili starijih). Iako tijekom kliničkih ispitivanja nisu uočene sveukupne razlike u učinkovitosti ili sigurnosti lijekova, povećana osjetljivost kod nekih starijih ispitanika ne može se isključiti s obzirom na mali broj ispitanih starijih pacijenata (vidjeti dio 5.2).
Za uporabu u djece mlađe od 12 godina i bolesnika s oštećenom funkcijom bubrega ili jetre, vidjeti dio 4.2.
Zbog prisutnosti laktoze monohidrata u tabletama od 10 mg rupatadina, pacijenti s rijetkim nasljednim problemima intolerancije na galaktozu, nedostatkom Lapp laktaze ili malapsorpcijom glukoze / galaktoze ne smiju uzimati ovaj lijek.
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija
Studije interakcija provedene su samo kod odraslih i adolescenata (starijih od 12 godina) s rupatadinom u tabletama od 10 mg.
Učinci drugih lijekova na rupatadin
Istodobnu primjenu sa snažnim inhibitorima CYP3A4 (npr. Itrakonazol, ketokonazol, vorikonazol, posakonazol, inhibitori proteaze HIV-a, klaritromicin, nefazodon) treba izbjegavati, a istodobnu primjenu s umjerenim inhibitorima CYP3A4 (eritromicin, flukonazol, diltiazem) treba koristiti s oprezom.
Istodobna primjena 20 mg rupatadina i ketokonazola ili eritromicina povećava sustavnu izloženost rupatadinu za 10 i 2-3 puta. Ove promjene nisu bile povezane s učinkom na QT interval niti s povećanjem nuspojava. do kada su se lijekovi davali odvojeno.
Interakcija sa sokom grejpa: Istodobna primjena soka od grejpa povećala je sistemsku izloženost rupatadinu 3,5 puta, stoga se ne smije davati istodobna primjena rupatadina sa sokom grejpa.
Učinci rupatadina na druge lijekove
Potreban je oprez pri istodobnoj primjeni rupatadina s drugim metaboliziranim lijekovima s uskim terapijskim prozorima jer je znanje o učinku rupatadina na druge lijekove ograničeno.
Interakcija s alkoholom: Nakon uzimanja alkohola, doza od 10 mg rupatadina imala je marginalne učinke u nekim psihomotornim testovima, iako se ti učinci nisu značajno razlikovali od onih uzrokovanih samo konzumacijom alkohola. Doza od 20 mg povećala je oštećenje uzrokovano unosom alkohola.
Interakcije s lijekovima koji potiskuju središnji živčani sustav: Kao i s drugim antihistaminicima, interakcije s depresorima središnjeg živčanog sustava ne mogu se isključiti.
Interakcija sa statinima: U kliničkim ispitivanjima provedenim s rupatadinom nije uobičajeno zabilježen asimptomatski porast CPK -a. Rizik od interakcija sa statinima, od kojih se neki također metaboliziraju izoenzimom citokroma P450 CYP3A4, nije poznat. Iz tog razloga rupatadin se mora koristiti oprezno kada se daje istodobno sa statinima.
04.6 Trudnoća i dojenje
Trudnoća
Dostupni su ograničeni podaci o uporabi rupatadina u trudnica. Studije na životinjama ne ukazuju na izravne ili neizravne štetne učinke na trudnoću, embrionalni / fetalni razvoj, porod ili postnatalni razvoj (vidjeti dio 5.3). poželjno je izbjegavati uporabu rupatadina tijekom trudnoće.
Vrijeme za hranjenje
Rupatadin se izlučuje u mlijeko životinja. Nije poznato izlučuje li se rupatadin u majčino mlijeko. Odluku o prekidu dojenja ili prekidu / prekidu terapije rupatadinom treba razmotriti uzimajući u obzir dobrobit dojenja za dijete i korist terapije za ženu.
Plodnost
Nema dostupnih kliničkih podataka o plodnosti. Studije na životinjama pokazale su značajno smanjenje plodnosti pri razinama izloženosti iznad onih primijećenih kod ljudi pri najvećoj terapijskoj dozi (vidjeti dio 5.3).
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima
Rupatadin 10 mg ne utječe na sposobnost upravljanja vozilima i rada sa strojevima.
Ipak, potreban je oprez prije upravljanja vozilima ili rada sa strojevima dok se ne utvrdi subjektivna reakcija pacijenta na rupatadin.
04.8 Nuspojave
U kliničkim ispitivanjima tablete od 10 mg rupatadina primijenjene su na više od 2025 odraslih i adolescenata, od kojih je 120 primalo rupatadin najmanje 1 godinu.
Najčešće nuspojave u kontroliranim kliničkim ispitivanjima bile su somnolencija (9,5%), glavobolja (6,9%) i umor (3,2%).
Većina nuspojava uočenih u kliničkim ispitivanjima bile su blage do umjerene jačine i općenito nisu zahtijevale prekid terapije.
Učestalosti nuspojava pripisuju se kako slijedi:
• Često (≥ 1 / 100a
• Manje često (≥ 1 / 1.000 a
• Rijetko (≥ 1/10 000 a
Učestalosti nuspojava prijavljenih u bolesnika liječenih rupatadinom u tabletama od 10 mg tijekom kliničkih ispitivanja i spontanih prijava bile su sljedeće:
• Infekcije i najezde
- Manje često: faringitis, rinitis.
• Poremećaji imunološkog sustava
- Rijetko: reakcije preosjetljivosti (uključujući anafilaktičke reakcije, angioedem i
urtikarija)*.
• Poremećaji metabolizma i prehrane
- Manje često: povećan apetit.
• Poremećaji živčanog sustava:
- Uobičajen: pospanost, glavobolja, vrtoglavica.
- Manje često: poremećaj pažnje.
• Srčani poremećaji
- Rijetko: tahikardija i lupanje srca *.
• Poremećaji disanja, prsnog koša i medijastinuma
- Manje često: epistaksa, suhoća nosa, kašalj, suhoća u grlu, orofaringealna bol.
• Gastrointestinalni poremećaji
- Uobičajen: suha usta
- Manje često: mučnina, bol u gornjem dijelu trbuha, proljev, dispepsija, povraćanje, bol u trbuhu, zatvor.
• Poremećaji kože i potkožnog tkiva
- Manje često: osip
• Poremećaji mišićno -koštanog sustava, vezivnog tkiva i kostiju
- Manje često: bolovi u leđima, artralgija, mijalgija.
• Opći poremećaji i stanja na mjestu primjene
- Uobičajen: umor, astenija.
- Manje često: žeđ, loš osjećaj, pireksija, razdražljivost.
• Dijagnostički testovi
- Manje često: povišena kreatin fosfokinaza u krvi, alanin aminotransferaza, aspartat aminotransferaza, poremećaji funkcije jetre, povećanje tjelesne težine.
* tahikardija, palpitacije i reakcije preosjetljivosti (uključujući anafilaktičke reakcije, angioedem i urtikariju) dogodile su se u razdoblju nakon stavljanja u promet tableta rupatadina od 10 mg.
Prijavljivanje sumnji na nuspojave
Izvještavanje o sumnji na nuspojave koje se jave nakon odobrenja lijeka važno je jer omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih djelatnika se traži da prijave sve sumnje na nuspojave putem nacionalnog sustava za prijavljivanje. "Adresa www. agenziafarmaco.gov.it/it/responsabili.
04.9 Predoziranje
Nisu zabilježeni slučajevi predoziranja. U kliničkoj studiji sigurnosti rupatadin u dnevnoj dozi od 100 mg u trajanju od 6 dana dobro se podnosio. Najčešća nuspojava bila je somnolencija. Ako se "dogodi slučajno unošenje vrlo visokih doza, potrebno je uvesti simptomatsko liječenje povezano s potrebnim mjerama potpore".
05.0 FARMAKOLOŠKA SVOJSTVA
05.1 Farmakodinamička svojstva
Farmakoterapijska skupina: drugi antihistaminici za sustavnu primjenu.
ATC oznaka: R06A X28.
Rupatadin je dugo djelujući antihistaminik druge generacije histaminskih antagonista druge generacije sa selektivnim djelovanjem na periferne antagoniste H1 receptora. Neki od metabolita (desloratadin i njegovi hidroksilirani metaboliti) zadržavaju antihistaminsko djelovanje i mogu djelomično pridonijeti ukupnoj učinkovitosti lijeka.
Studije in vitro provedene s rupatadinom u visokim koncentracijama pokazale su inhibiciju degranulacije mastocita uzrokovanu imunološkim i neimunološkim podražajima te inhibiciju oslobađanja citokina, posebno TNFa u ljudskim mastocitima i monocitima.
Kliničku važnost ovih opažanja tek treba potvrditi.
Klinička ispitivanja na dobrovoljcima (n = 375) i bolesnicima (n = 2650) s alergijskim rinitisom i kroničnom idiopatskom urtikarijom nisu pokazala značajniji učinak na elektrokardiogram kada se rupatadin primjenjivao u dozama između 2 mg i 100 mg.
Kronična idiopatska urtikarija proučavana je kao klinički model za stanja slična urtikariji budući da je temeljna patofiziologija slična, ne uzimajući u obzir etiologiju, a također i zato što se kronični bolesnici na kraju mogu lakše regrutirati. Budući da je oslobađanje histamina uzrok svih bolesti sličnih urtikariji, očekuje se da će rupatadin biti učinkovit u ublažavanju simptoma drugih kliničkih stanja, poput urtikarije, uz kroničnu idiopatsku urtikariju, kako je predloženo u kliničkim smjernicama.
U placebom kontroliranom kliničkom ispitivanju u bolesnika s kroničnom idiopatskom urtikarijom, rupatadin je bio učinkovit u smanjenju prosječne ocjene svrbeža od početne vrijednosti tijekom razdoblja liječenja od 4 tjedna (promjene u odnosu na početnu vrijednost: rupatadin 57,5%, placebo 44,9%) i u smanjenju srednje vrijednosti broj pšenice (54,3% prema 39,7%).
05.2 Farmakokinetička svojstva
Apsorpcija i bioraspoloživost
Rupatadin se brzo apsorbira nakon oralne primjene, s Tmax od približno 0,75 sati nakon doziranja. Prosječni Cmax je 2,6 ng / ml nakon primjene pojedinačne oralne doze od 10 mg i 4,6 ng / ml nakon pojedinačne oralne doze od 20 mg. Farmakokinetika rupatadina je linearna za dozu između 10 i 20 mg nakon pojedinačne i ponovljene primjene doze. Nakon doze od 10 mg jednom dnevno tijekom 7 dana, srednji Cmax je 3,8 ng / mL.
Koncentracija u plazmi smanjila se bi-eksponencijalno sa prosječnim poluvrijeme eliminacije od 5,9 sati. Stopa vezanja rupatadina za proteine plazme je 98,5-99%.
Budući da se rupatadin nikada nije intravenozno primjenjivao na ljudima, nema podataka o njegovoj apsolutnoj bioraspoloživosti.
Učinci unosa hrane
Unos hrane povećava sustavnu izloženost (AUC) rupatadinu za približno 23%.
Izloženost jednom od njegovih aktivnih metabolita i glavnom neaktivnom metabolitu je praktički ista (približno 5% odnosno 3% smanjenje). Vrijeme potrebno za postizanje maksimalne koncentracije rupatadina u plazmi (Tmax) odgođeno je 1 sat. Maksimalna plazma unos hrane nije utjecao na koncentraciju (Cmax). Ove razlike nemaju klinički značaj.
Metabolizam i eliminacija
U studiji izlučivanja na ljudima (40 mg 14C-rupatadina), 34,6% primijenjene radioaktivnosti pronađeno je u urinu, a 60,9% u izmetu povučeno u roku od 7 dana. Rupatadin se podvrgava značajnom predsistemskom metabolizmu kada se daje oralno. količina nepromijenjene djelatne tvari u urinu i izmetu bila je zanemariva.
To znači da se rupatadin gotovo potpuno metabolizira.
Otprilike, aktivni metaboliti desloratadin i drugi hidroksilirani derivati činili su 27% odnosno 48% ukupne sistemske izloženosti aktivnih tvari.
Obrazovanje in vitro na metabolizam u mikrosomima ljudske jetre ukazuju da se rupatadin primarno metabolizira citokromom P450 (CYP 3A4).
Određene skupine pacijenata
U studiji provedenoj na zdravim dobrovoljcima koja je uspoređivala rezultate kod mladih odraslih osoba i starijih pacijenata, vrijednosti AUC i Cmax za rupatadin bile su veće u starijih osoba nego u mladih odraslih osoba. Vjerojatno je to posljedica smanjenja metabolizma jetre u prvom prolazu starije osobe. Takve razlike nisu uočene u ispitivanim metabolitima. Prosječno poluvrijeme eliminacije rupatadina u starijih i mladih dobrovoljaca bilo je 8,7 sati, odnosno 5,9 sati. Budući da ti rezultati za rupatadin i njegove metabolite nisu bili klinički značajni, zaključeno je da nije potrebna prilagodba za uporabu doze od 10 mg u starijih osoba.
05.3 Pretklinički podaci o sigurnosti
Neklinički podaci ne otkrivaju posebnu opasnost za ljude na temelju konvencionalnih farmakoloških studija, toksičnosti pri ponovljenim dozama, genotoksičnosti i kancerogenog potencijala.
Doza veća od 100 puta klinički preporučene doze (10 mg) rupatadina nije produljila QTc ili QRS interval niti uzrokovala aritmiju kod različitih životinjskih vrsta, poput štakora, zamoraca i pasa. Rupatadin je jedan od njegovih glavnih. Aktivni metaboliti u ljudi, 3-hidroksidesloratadin nije utjecao na srčani akcijski potencijal u izoliranim psećim Purkinjeovim vlaknima u koncentracijama koje su bile najmanje 2000 puta veće od Cmax postignute nakon primjene doze od 10 mg u ljudi. U studiji koja je procjenjivala učinak na klonirani humani HERG kanal, rupatadin je inhibirao kanal u koncentraciji 1685 puta većoj od Cmax dobivene nakon primjene 10 mg rupatadina. Desloratadin, metabolit s najvećom aktivnošću, nije imao učinka u koncentraciji od 10 mikromolara. Studije distribucije tkiva s radioaktivno obilježenim rupatadinom na štakorima pokazale su da se rupatadin ne nakuplja u srčanom tkivu.
Studije plodnosti na štakorima pokazale su značajno smanjenje plodnosti mužjaka i ženki u dozi od 120 mg / kg / dan, što je rezultiralo Cmax rupatadina 268 puta većim od onog postignutog nakon primjene terapijske doze kod ljudi (10 mg / dan) . umrijeti). Fetalna toksičnost (kašnjenje u razvoju, nepotpuno okoštavanje, manje promjene na skeletu) pokazana je u štakora samo u majčinskim toksičnim dozama (25 i 120 mg / kg / dan).
Kod kunića nije pokazana razvojna toksičnost za doze do 100 mg / kg. Razine doza pri kojima nisu uočeni štetni učinci na razvoj (NOAEL) identificirane su pri 5 mg / kg / dan u štakora i 100 mg / kg / dan u kunića, čime je postignut Cmax od 45 odnosno 116 puta veći od toga mjereno u muškaraca u terapijskim dozama (10 mg / dan).
06.0 FARMACEUTSKE INFORMACIJE
06.1 Pomoćne tvari
Predželatinizirani kukuruzni škrob
Mikrokristalna celuloza
Crveni željezov oksid (E-172)
Žuti željezov oksid (E-172)
Laktoza monohidrat
Magnezijev stearat
06.2 Nekompatibilnost
Nije bitno.
06.3 Razdoblje valjanosti
3 godine.
06.4 Posebne mjere pri skladištenju
Čuvajte blister u vanjskom pakiranju kako biste zaštitili lijek od svjetlosti.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja
PVC / PVDC / aluminijski mjehurići.
Pakiranja od 3, 7, 10, 15, 20, 30, 50 i 100 tableta. Ne mogu se na tržište staviti sve veličine pakiranja.
06.6 Upute za uporabu i rukovanje
Nema posebnih uputa.
Neiskorišteni lijekovi i otpad nastali iz ovog lijeka moraju se zbrinuti u skladu s lokalnim propisima.
07.0 Nositelj odobrenja za stavljanje u promet
J. Uriach & Cía., S.A.
Av. Camí Reial, 51-57
08184 Palau-solità i Plegamans (Španjolska)
Prodavač: Recordati S.p.A. - Milane
08.0 BROJ DOZVOLE ZA PROMET
AIC n. 037880010 "Tablete od 10 mg" 3 tablete u PVC / PVDC / Al blisteru
AIC n. 037880022 "10 mg tablete" 7 tableta u PVC / PVDC / Al blisteru
AIC n. 037880034 "Tablete od 10 mg" 10 tableta u PVC / PVDC / Al blisteru
AIC n. 037880046 "Tablete od 10 mg" 15 tableta u PVC / PVDC / Al blisteru
AIC n. 037880059 "Tablete od 10 mg" 20 tableta u PVC / PVDC / Al blisteru
AIC n. 037880061 "10 mg tablete" 30 tableta u PVC / PVDC / Al blisteru
AIC n. 037880073 "Tablete od 10 mg" 50 tableta u PVC / PVDC / Al blisteru
AIC n. 037880085 "10 mg tablete" 100 tableta u PVC / PVDC / Al blisteru
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA
Datum prve autorizacije: 13. lipnja 2008
Datum obnove: 11. ožujka 2011












.jpg)